Эмпиема плевры - Pleural empyema
| Эмпиема плевры | |
|---|---|
| Другие имена | Пиоторакс, гнойный плеврит, эмпиема легких |
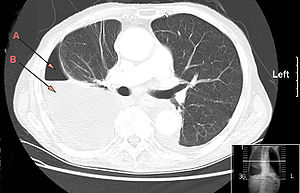 | |
| КТ грудной клетки показывает большую правую сторону гидропневмоторакс из плевры эмпиема. Стрелки A: воздух, B: жидкость | |
| Специальность | Пульмонология, кардиоторакальная хирургия |
| Симптомы | Лихорадка, боль в груди при вдохе, кашель, одышка |
| Причины | Бактерии (часто стрептококковая пневмония) |
| Диагностический метод | Рентген грудной клетки, УЗИ, КТ, торакоцентез |
| Дифференциальная диагностика | Пневмония, плевральный выпот, легочная эмболия |
| Уход | Поддерживающая терапия, антибиотики, хирургия, грудная трубка |
Эмпиема плевры это собрание гной в плевральная полость вызванный микроорганизмы, обычно бактерии.[1] Часто это происходит в контексте пневмония, травма или операция на груди.[1] Это один из различных видов плевральный выпот. Выделяют три стадии: экссудативная, когда наблюдается увеличение плевральная жидкость с наличием гноя или без него; фибрино-гнойный, когда фиброзные перегородки образуют локализованные гнойные карманы; и заключительный этап организации, когда происходит рубцевание плевральных оболочек с возможной неспособностью легкого расширяться. Простой плевральный выпот встречается до 40% бактериальных пневмоний. Обычно они небольшие и проходят при соответствующей антибактериальной терапии. Если же эмпиема развивается, требуется дополнительное вмешательство.
Признаки и симптомы
Клиническая картина как взрослого, так и педиатрического пациента с эмпиемой плевры зависит от нескольких факторов, в том числе от возбудителя. Большинство случаев проявляется в условиях пневмонии, хотя до одной трети пациентов не имеют клинических признаков пневмонии, и до 25% случаев связаны с травмой (включая хирургическое вмешательство).[2] Типичные симптомы включают: кашель, грудная боль, одышка и высокая температура.[нужна цитата ]
Диагностика
Первоначальные исследования при подозрении на эмпиему остаются рентгенограмма грудной клетки, хотя он не может отличить эмпиему от неинфицированного парапневмонического выпота.[3] УЗИ должен использоваться для подтверждения наличия скопления плевральной жидкости и может использоваться для оценки размера выпота, различения свободной и локализованной плевральной жидкости и направления торакоцентез если необходимо. Грудь CT и МРТ не предоставляют дополнительной информации в большинстве случаев и поэтому не должны выполняться в плановом порядке.[4] На КТ жидкость эмпиемы чаще всего имеет радиоплотность около 0-20 Единицы Хаунсфилд (HU),[5] но становится более 30 HU, когда со временем уплотняется.[6]
Наиболее часто используемые «золотые» критерии эмпиемы - плевральный выпот с макроскопическим наличием гноя, положительный Окраска по Граму или посев плевральной жидкости, или рН плевральной жидкости ниже 7,2 при нормальном рН периферической крови.[7][8] Таким образом, клинические рекомендации для взрослых пациентов рекомендуют диагностическую аспирацию плевральной жидкости у пациентов с плевральным выпотом в сочетании с сепсис или легочная болезнь.[9] Поскольку плевральный выпот у детей почти всегда парапневмонический, и грудная трубка дренирование может быть выполнено по клиническим причинам, британские руководящие принципы лечения плевральной инфекции у детей не рекомендуют диагностический забор образцов плевральной жидкости.[4]
Кровь и посев мокроты часто уже проводилась в условиях внебольничной пневмонии, требующей госпитализации. Однако следует отметить, что микроорганизм, ответственный за развитие эмпиемы, не обязательно совпадает с организмом, вызывающим пневмонию, особенно у взрослых. Как уже упоминалось ранее, чувствительность посев плевральной жидкости обычно низкий, часто частично из-за предшествующего приема антибиотиков. Было показано, что выход посевов может быть увеличен с 44% до 69%, если плевральная жидкость вводится в бутыли для культур крови (аэробных и анаэробных) сразу после аспирации.[8] Кроме того, можно улучшить диагностические показатели для конкретных патогенов, используя полимеразной цепной реакции или обнаружение антигена, особенно для Streptococcus pneumoniae, Streptococcus pyogenes и Staphylococcus aureus. В исследовании, в котором участвовали 78 детей с эмпиемой плевры, возбудитель болезни мог быть идентифицирован с помощью прямого посева свежей плевральной жидкости у 45% пациентов, а еще у 28% пациентов с помощью ПЦР на плевральной жидкости отрицательных культур.[10] Обнаружение пневмококкового антигена в образцах плевральной жидкости с помощью латексной агглютинации также может быть полезно для быстрой диагностики пневмококковой эмпиемы. В ранее упомянутом исследовании положительная и отрицательная прогностическая ценность обнаружения пневмококкового антигена составила 95% и 90% соответственно.[10] Однако, несмотря на дополнительную диагностическую ценность этих тестов, ПЦР и определение антигена имеют ограниченное значение при определении выбора лечения из-за отсутствия информации о устойчивость к антибиотикам.[нужна цитата ]
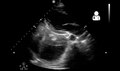
Эмпиема плевры на УЗИ[11]
Эмпиема плевры на УЗИ[11]
Эмпиема плевры на УЗИ[11]
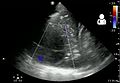
Эмпиема плевры на УЗИ[11]
Уход
Дренаж плевральной жидкости
Доказанная эмпиема (согласно «золотым» критериям, упомянутым ранее) является показанием для быстрого грудная трубка дренаж.[9] Было показано, что это улучшает разрешение инфекции и сокращает время госпитализации.[12] Данные метаанализа показали, что pH плевральной жидкости <7,2 является наиболее убедительным показателем для прогнозирования необходимости дренирования плевральной дренажной трубки у пациентов с негнойной жидкостью с отрицательным посевом.[13] Другие показания для дренирования включают плохой клинический прогресс во время лечения только антибиотиками и пациентов с локализованным плевральным скоплением.[нужна цитата ]
Из-за вязкой, бугристой природы инфицированной плевральной жидкости в сочетании с возможной перегородкой и локализацией было предложено, чтобы внутриплевральная фибринолитический или же муколитический терапия может улучшить дренаж и, следовательно, может положительно повлиять на клинический результат.[14] Внутриплевральный фибринолиз с урокиназа снизилась потребность в хирургическом вмешательстве, но наблюдается тенденция к усилению серьезных побочных эффектов.[15]
Примерно от 15 до 40 процентов людей нуждаются в хирургическом дренировании инфицированной плевральной полости из-за неадекватного дренажа из-за закупорки грудной трубки или локализованной эмпиемы.[16] Таким образом, пациенты должны быть рассмотрены для операции, если у них сохраняются признаки сепсиса в сочетании с постоянным скоплением плевры, несмотря на дренаж и антибиотики.[9] Видеоассистированная торакоскопическая хирургия (VATS) используется в качестве терапии первой линии во многих больницах, хотя открытый грудной дренаж остается часто используемой альтернативной техникой.[нужна цитата ]
Антибиотики
Нет доступных данных о способе введения и продолжительности приема антибиотиков у пациентов с эмпиемой плевры. Специалисты сходятся во мнении, что всех пациентов следует госпитализировать и лечить антибиотиками внутривенно.[4][9] Конкретный противомикробный агент следует выбирать на основе окрашивания по Граму и посева или на основе местных эпидемиологических данных, если они недоступны. Анаэробное покрытие должно быть включено у всех взрослых и детей, если: стремление похоже. Сообщалось о хорошем проникновении плевральной жидкости и эмпиеме у взрослых при пенициллины, цефтриаксон, метронидазол, клиндамицин, ванкомицин, гентамицин и ципрофлоксацин.[17][18] Аминогликозиды обычно следует избегать, поскольку они плохо проникают в плевральную полость. Нет четкого консенсуса относительно продолжительности внутривенной и пероральной терапии. Переход на пероральные антибиотики можно рассматривать после клинического и объективного улучшения (адекватный дренаж и удаление плевральной дренажной трубки, снижение CRP, нормализация температуры). Затем пероральное лечение антибиотиками следует продолжить еще в течение 1–4 недель, опять же в зависимости от клинической, биохимической и радиологической реакции.[4][9]
Прогноз
Всем пациентам с эмпиемой требуется амбулаторное наблюдение с повторной рентгенологией грудной клетки и биохимическим анализом воспаления в течение 4 недель после выписки. Рентгенограмма грудной клетки нормализуется у большинства пациентов к 6 месяцам. Пациентам, конечно, следует рекомендовать вернуться раньше, если симптомы возобновятся. Отдаленные последствия эмпиемы плевры редки, но включают: бронхоплевральный свищ образование, рецидивирующая эмпиема и утолщение плевры, которые могут привести к функциональному нарушению легких, требующему хирургического вмешательства. декортикация.[9]
Примерно 15% взрослых пациентов с плевральной инфекцией умирают в течение 1 года после события, хотя смерть обычно происходит из-за сопутствующих заболеваний, а не непосредственно из-за сепсиса из-за эмпиемы.[нужна цитата ] Смертность у детей обычно составляет менее 3%.[4] Никакие надежные клинические, радиологические характеристики или характеристики плевральной жидкости точно не определяют прогноз пациента при первичном обращении.[19]
Эпидемиология
Частота эмпиемы плевры и распространенность конкретных возбудителей болезни варьируется в зависимости от источника инфекции (внебольничная пневмония или пневмония, приобретенная в больнице), возраста пациента и иммунного статуса хозяина. Факторы риска включают: алкоголизм, употребление наркотиков, ВИЧ-инфекция, новообразование и ранее существовавшие легочная болезнь.[20] Эмпиема плевры была обнаружена у 0,7% из 3675 пациентов, нуждающихся в госпитализации по поводу внебольничной пневмонии в недавнем одноцентровом проспективном исследовании в Канаде.[7] Многоцентровое исследование, проведенное в Великобритании с участием 430 взрослых пациентов с внебольничной эмпиемой плевры, выявило отрицательные посевы плевральной жидкости у 54% пациентов. Группа Streptococcus milleri в 16%, Золотистый стафилококк в 12%, Пневмококк в 8%, прочие Стрептококки в 7% и анаэробные бактерии в 8%.[14] Учитывая трудности культивирования анаэробных бактерий, частота последних (включая смешанные инфекции) может быть недооценена.
Риск эмпиемы у детей сопоставим со взрослыми. Используя базу данных детских стационаров Соединенных Штатов, заболеваемость среди детей, госпитализированных по поводу внебольничной пневмонии, составляет около 1,5%.[21] хотя в отдельных больницах зарегистрирован процент до 30%,[22] различие, которое можно объяснить временным эндемическим заболеванием высокоинвазивных серотип или гипердиагностика небольших парапневмонических выпотов. Распределение возбудителей действительно сильно отличается от такового у взрослых: при анализе 78 детей с внебольничной эмпиемой плевры у 27% пациентов не было обнаружено никаких микроорганизмов. Пневмококк в 51%, Streptococcus pyogenes в 9% и Золотистый стафилококк в 8%.[10]
Несмотря на то что пневмококковая вакцинация резко снизилась заболеваемость пневмонией у детей, это не повлияло на частоту осложненной пневмонии. Было показано, что заболеваемость эмпиемой у детей росла уже в конце 20-го века, и что широкое использование пневмококковой вакцины не замедлило эту тенденцию.[23] Частично это можно объяснить изменением распространенности (более инвазивной) пневмококковой инфекции. серотипы, некоторые из которых не покрываются вакциной, а также рост заболеваемости пневмонией, вызванной другими стрептококками и стафилококками.[24] Заболеваемость эмпиемой, кажется, растет и среди взрослого населения, хотя и более медленными темпами.
Рекомендации
- ^ а б Redden MD, Chin TY, van Driel ML (март 2017 г.). «Хирургическое и нехирургическое лечение эмпиемы плевры». Кокрановская база данных Syst Rev. 3: CD010651. Дои:10.1002 / 14651858.CD010651.pub2. ISSN 1469-493X. ЧВК 6464687. PMID 28304084.
- ^ Фернандес-Котарело М.Дж., Лопес-Медрано Ф., Сан-Хуан Р., Диас-Педроче С., Лизасоайн М., Чавес Ф., Агуадо Дж. М. (март 2007 г.). «Белковые проявления эмпиемы плевры, вызванной Streptococcus pneumoniae, у взрослых». Евро. J. Intern. Med. 18 (2): 141–5. Дои:10.1016 / j.ejim.2006.09.017. PMID 17338967.
- ^ Кинг С., Томсон А. (2002). «Радиологические перспективы при эмпиеме». Британский медицинский бюллетень. 61: 203–14. Дои:10.1093 / bmb / 61.1.203. PMID 11997307.
- ^ а б c d е Бальфур-Линн И.М., Абрахамсон Э., Коэн Дж., Хартли Дж., Кинг С., Парих Д., Спенсер Д., Томсон А. Х., Уркхарт Д. (2005). «Рекомендации BTS по лечению плевральной инфекции у детей». Грудная клетка. 60 (Дополнение 1): 1–21. Дои:10.1136 / thx.2004.030676. ЧВК 1766040. PMID 15681514.
- ^ Йылдыз С., Сесе Х, Тюрксой О. (октябрь 2010 г.). «Дискриминационная роль КТ при экссудативных и транссудативных плевральных выпотах». AJR Am J Roentgenol. 195 (4): W305, ответ автора W306. Дои:10.2214 / AJR.10.4437. ISSN 0361-803X. PMID 20858794.
- ^ Моше Шейн, Джон К. Маршалл (2013). Контроль источников: руководство по лечению хирургических инфекций. Springer Science & Business Media. ISBN 9783642559143.
- ^ а б Ахмед Р., Марри Т., Хуанг Дж. (2006). «Эмпиема грудной клетки у больных внебольничной пневмонией». Американский журнал медицины. 119 (10): 877–83. Дои:10.1016 / j.amjmed.2006.03.042. PMID 17000220.
- ^ а б Феррер А., Оссет Дж., Алегре Дж., Суриньях Дж. М., Креспо Е., Фернандес де Севилья Т., Фернандес Ф. (апрель 1999 г.). «Проспективное клинико-микробиологическое исследование плевральных выпотов». Евро. J. Clin. Microbiol. Заразить. Дис. 18 (4): 237–41. Дои:10.1007 / с100960050270. PMID 10385010.
- ^ а б c d е ж Дэвис Х, Дэвис Р., Дэвис С. (2010). «Ведение плевральной инфекции у взрослых: Руководство Британского торакального общества по заболеваниям плевры, 2010 г.». Грудная клетка. 65 (Дополнение 2): 41–53. Дои:10.1136 / thx.2010.137000. PMID 20696693.
- ^ а б c Ле Монье А., Карбоннель Е., Захар Дж. Р., Ле Буржуа М., Абачин Е., Кен Дж., Варон Е., Декамп П., Де Блик Дж., Шейнман П., Берше П., Феррони А. (2006). «Микробиологическая диагностика эмпиемы у детей: сравнительные оценки посевом, полимеразной цепной реакцией и обнаружением пневмококкового антигена в плевральной жидкости». Клинические инфекционные болезни. 42 (8): 1135–40. Дои:10.1086/502680. PMID 16575731.
- ^ а б c d «UOTW # 28 - УЗИ недели». УЗИ недели. 3 декабря 2014 г.. Получено 27 мая 2017.
- ^ Сассе С., Нгуен Т.К., Маллиган М., Ван Н.С., Махутте С.К., Light RW (июнь 1997 г.). «Влияние раннего размещения дренажной трубки на разрешение эмпиемы». Грудь. 111 (6): 1679–83. Дои:10.1378 / сундук.111.6.1679. PMID 9187193.
- ^ Хеффнер Дж. Э., Браун Л. К., Барбьери С., ДеЛео Дж. М. (июнь 1995 г.). «Химический анализ плевральной жидкости при парапневмонических выпотах. Мета-анализ». Являюсь. J. Respir. Крит. Care Med. 151 (6): 1700–8. Дои:10.1164 / ajrccm.151.6.7767510. PMID 7767510.
- ^ а б Маскелл Н.А., Дэвис К.В., Нанн А.Дж., Хедли Е.Л., Глисон Ф.В., Миллер Р., Гейб Р., Рис Г.Л., Пето Т.Е., Вудхед М.А., Лейн DJ, Дарбишир Дж. Х., Дэвис Р.Дж. (2005). «Управляемое в Великобритании исследование интраплевральной стрептокиназы при плевральной инфекции». Медицинский журнал Новой Англии. 352 (9): 865–74. Дои:10.1056 / nejmoa042473. PMID 15745977.
- ^ Не В., Лю И, Йе Дж, Ши Л., Шао Ф, Ин К., Чжан Р. (июль 2014 г.). «Эффективность внутриплевральной инстилляции фибринолитиков для лечения эмпиемы плевры и парапневмонического выпота: метаанализ рандомизированных контрольных исследований». Clin Respir J. 8 (3): 281–91. Дои:10.1111 / crj.12068. PMID 24428897.
- ^ Фергюсон А.Д., Прескотт Р.Дж., Селкон Дж. Б., Уотсон Д., Суинберн С. Р. (апрель 1996 г.). «Клиническое течение и лечение эмпиемы грудной клетки». QJM. 89 (4): 285–9. Дои:10.1093 / qjmed / 89.4.285. PMID 8733515.
- ^ Тейшейра Л. Р., Сассе С. А., Вилларино М. А., Нгуен Т., Маллиган М. Е., Light RW (июнь 2000 г.). «Уровни антибиотиков в эмпиемической плевральной жидкости». Грудь. 117 (6): 1734–9. Дои:10.1378 / сундук.117.6.1734. PMID 10858410.
- ^ Умут С., Демир Т., Аккан Г., Кескинер Н., Йилмаз В., Йилдирим Н., Сипахиоглу Б., Хасан А., Барлас А., Сезер К. (апрель 1993 г.). «Проникновение ципрофлоксацина в плевральную жидкость». J Chemother. 5 (2): 110–2. Дои:10.1080 / 1120009X.1993.11739217. PMID 8515292.
- ^ Дэвис К.В., Кирни С.Е., Глисон Ф.В., Дэвис Р.Дж. (ноябрь 1999 г.). «Предикторы исхода и долгосрочной выживаемости у пациентов с плевральной инфекцией». Являюсь. J. Respir. Крит. Care Med. 160 (5, п. 1): 1682–7. Дои:10.1164 / ajrccm.160.5.9903002. PMID 10556140.
- ^ Альфагеме I, Муньос Ф., Пенья Н., Умбрия С. (март 1993 г.). «Эмпиема грудной клетки у взрослых. Этиология, микробиологические данные и лечение». Грудь. 103 (3): 839–43. Дои:10.1378 / сундук.103.3.839. PMID 8449078.
- ^ Ли С., Танкреди Д. (2010). «Несмотря на пневмококковую конъюгированную вакцину, у детей в США увеличилось количество госпитализаций при эмпиеме». Педиатрия. 125 (1): 26–33. Дои:10.1542 / педс.2009-0184. PMID 19948570.
- ^ Байингтон С.Л., Спенсер Л.И., Джонсон Т.А., Павия А.Т., Аллен Д., Мейсон Е.О., Каплан С., Кэрролл К.С., Дейли Дж.А., Кристенсон Дж. К., Самор М. Х. (2002). «Эпидемиологическое исследование стабильно высокого уровня детской парапневмонической эмпиемы: факторы риска и микробиологические ассоциации». Клинические инфекционные болезни. 34 (4): 434–40. Дои:10.1086/338460. PMID 11797168.
- ^ Гриджалва К.Г., Нуорти Дж. П., Чжу Й., Гриффин М. Р. (2010). «Рост заболеваемости эмпиемой, осложняющей внебольничную пневмонию у детей в США». Клинические инфекционные болезни. 50 (6): 805–13. Дои:10.1086/650573. ЧВК 4696869. PMID 20166818.
- ^ Обандо I, Камачо-Ловилло М.С., Поррас А., Гандиа-Гонсалес М.А., Молинос А., Васкес-Барба И., Морилло-Гутьеррес Б., Нет О.В., Тарраго Д. (август 2012 г.). «Устойчиво высокая распространенность пневмококка серотипа 1 в детской парапневмонической эмпиеме на юге Испании с 2005 по 2009 год». Clin. Microbiol. Заразить. 18 (8): 763–8. Дои:10.1111 / j.1469-0691.2011.03632.x. PMID 21910779.
внешняя ссылка
| Классификация | |
|---|---|
| Внешние ресурсы |