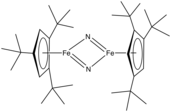
Металл нитридокомплекс - Metal nitrido complex
Нитридокомплексы металлов находятся координационные соединения и металлические кластеры которые содержат атом азота, связанный только с переходными металлами. Эти соединения молекулярный, т.е. дискретный в отличие от полимерного, плотный нитрид материалы, которые полезны в материаловедение.[1] Различие между молекулярными и твердотельными полимерами не всегда очень четкое, о чем свидетельствуют материалы Li6Мин4 и более конденсированные производные, такие как Na3Мин3. Нитридокомплексы переходных металлов вызывают интерес отчасти потому, что предполагается, что азотфиксация протекает через промежуточные нитридо. Нитридокомплексы известны давно, первым примером являются соли [OsO3N]−, описанный в 19 веке.[2]
Структурные тенденции
Мононуклеарные комплексы содержат концевые нитридные лиганды, обычно с короткими расстояниями M-N, соответствующими металлический лиганд множественные связи. Например, в анионе в PPh4 [MoNCl4], расстояние Пн-С составляет 163,7 пм. Появление концевых нитридолигандов соответствует паттернам, наблюдаемым для оксокомплексов: они более характерны для ранних и более тяжелых металлов. Известно много би- и полиядерных комплексов с мостиковыми нитридолигандами.[3] Возможны также более экзотические нитридокомплексы металлов, такие как недавно описанное соединение, содержащее концевую нитридную связь урана (-U≡N).[4]
- Примеры нитридокомплексов металлов

[ОсНО3]−, который изоэлектронен четырехокись осмия.

[MoNCl4]−, квадратно-пирамидальный комплекс Mo (VI).

[W2(мк-N) Cl10]−, содержащий два центра W (VI), соединенных мостиком нитридолиганда.

[Ir3N (SO4)6(ЧАС2O)3]4−, структурно связанные с основной ацетат железа.

Нитридокомплекс урана.
Подготовительные маршруты
Нитриды металлов производятся с использованием различных источников азота. Первый пример был подготовлен из амид (NH2−) как тогда3− источник:
- OsO4 + KNH2 → КОСО3N + H2О
Однако чаще всего нитридо комплексы производятся из азидокомплексов ..[5] Движущей силой этих реакций является высокая стабильность N2. Трихлорид азота является эффективным реагентом для образования хлор-нитридокомплексов. В некоторых случаях даже N2 и нитрилы могут служить источниками нитридных лигандов.
Реакции нитридолигандов
Нитридный лиганд может быть как электрофильным, так и нуклеофильным.[6][7] Конечные нитриды ранних металлов имеют тенденцию быть основными и окисляемыми, тогда как нитриды более поздних металлов имеют тенденцию быть окисляющими и электрофильными. Первое поведение иллюстрируется их N-протонирование и н-алкилирование. Нитридокомплексы Ru и Os часто добавляют органофосфины для получения производных иминофосфина, содержащих R3PN− лиганд.
Межузельные нитриды
Благодаря способности нитридолигандов служить мостиковый лиганд известно, что несколько металлических кластеров содержат в центре нитридные лиганды. Такие нитридо-лиганды называют межстраничный. В некоторых случаях нитрид полностью заключен в центр из шести или более металлов и не может вступать в реакции, хотя он способствует образованию интерметаллических связей.[8]

Общие ссылки
- ^ Гринвуд, Норман Н.; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн. ISBN 978-0-08-037941-8.
- ^ Fritzsche, J .; Струве, Х. (1847). "Ueber die Osman-Osmiumsäure". Journal für Praktische Chemie. 41 (1): 97–113. Дои:10.1002 / prac.18470410113.
- ^ Дехнике, Курт; Стрэле, Иоахим (1992). «Нитридокомплексы переходных металлов». Angewandte Chemie International Edition на английском языке. 31 (8): 955–978. Дои:10.1002 / anie.199209551.
- ^ King, David M .; Тунец, Флориана; Макиннес, Эрик Дж. Л .; Макмастер, Джонатан; Льюис, Уильям; Блейк, Александр Дж .; Лиддл, Стивен Т. (2012). «Синтез и структура конечного нитридного комплекса урана». Наука. 337 (6095): 717–720. Bibcode:2012Наука ... 337..717K. Дои:10.1126 / science.1223488. PMID 22745250.
- ^ Райнерс, Матиас; Маэкава, Миюки; Данилюк, Константин Г .; Фрейтаг, Матиас; Джонс, Питер Дж .; Белый, Питер С .; Хоэнбергер, Йоханнес; Саттер, Йорг; Мейер, Карстен; Марон, Лоран; Уолтер, Марк Д. (2017). «Исследования реакционной способности [Cp'Fe (μ-I)] 2: комплексы нитридо-, сульфидо- и диселенидного железа, полученные в результате активации псевдогалогенидом». Химическая наука. 8 (5): 4108–4122. Дои:10.1039 / C7SC00570A. ЧВК 6099922. PMID 30155215.
- ^ Дехнике, Курт; Веллер, Франк; Стрэле, Иоахим (2001). «Нитридные мостики между переходными металлами и элементами основной группы, проиллюстрированные сериями от [M] NNa до [M] NCl». Chem. Soc. Rev. 30 (2): 125–135. Дои:10.1039 / a802635a.
- ^ Смит, Джереми М. (2014). Реактивные комплексы нитридов переходных металлов. Прогресс в неорганической химии. 58. С. 417–470. Дои:10.1002 / 9781118792797.ch06. ISBN 9781118792797.
- ^ Гладфельтер, Уэйн Л. (1985). Металлоорганические кластеры металлов, содержащие нитрозильные и нитридо-лиганды. Успехи металлоорганической химии. 24. С. 41–86. Дои:10.1016 / S0065-3055 (08) 60413-X. ISBN 9780120311248.