Смешанное кислотное брожение - Mixed acid fermentation
Смешанное кислотное брожение это биологический процесс, с помощью которого шестиуглеродный сахар, например глюкоза превращается в сложную и изменчивую смесь кислот. Это анаэробный ферментация реакция, распространенная у бактерий. Это характерно для членов Энтеробактерии, большое семейство грамотрицательных бактерий, которое включает Кишечная палочка.[3]
Смесь конечных продуктов смешанного кислотного брожения включает: лактат, ацетат, сукцинат, форматировать, этиловый спирт а газы H2 и CO2. Формирование этих конечных продуктов зависит от наличия определенных ключевых ферменты в бактерии. Пропорция, в которой они образуются, варьируется у разных видов бактерий.[4] Путь смешанной кислотной ферментации отличается от других путей ферментации, которые производят меньше конечных продуктов в фиксированных количествах. Конечные продукты смешанного кислотного брожения могут найти множество полезных применений в биотехнология и промышленность. Например, этанол широко используется в качестве биотопливо.[5] Таким образом, были обнаружены множественные бактериальные штаммы. метаболически сконструированный в лаборатории для увеличения индивидуального дает определенных конечных продуктов.[2] Это исследование проводилось в основном в Кишечная палочка и продолжается.
Смешанное кислотное брожение в Кишечная палочка
Кишечная палочка использовать пути брожения в качестве последнего варианта для энергетического обмена, поскольку они производят очень мало энергии по сравнению с дыханием.[6] Смешанное кислотное брожение в Кишечная палочка происходит в два этапа. Эти этапы описаны в биологической базе данных для Кишечная палочка, EcoCyc.[1]
Первый из этих двух этапов - это реакция гликолиза. В анаэробных условиях происходит реакция гликолиза, при которой глюкоза превращается в пируват:
глюкоза → 2 пируват
Чистое производство 2 АТФ и 2 НАДН молекул на молекулу превращенной глюкозы. АТФ генерируется фосфорилирование на уровне субстрата. НАДН образуется из снижение НАД.
На второй стадии пируват, полученный гликолизом, превращается в один или несколько конечных продуктов с помощью следующих реакций. В каждом случае обе молекулы НАДН, образующиеся при гликолизе, являются повторно окисленный в НАД+. Каждый альтернативный путь требует отдельного ключевого фермента в Кишечная палочка. После того, как эти пути образуют различные количества различных конечных продуктов, они секретируются из клетки.[1]
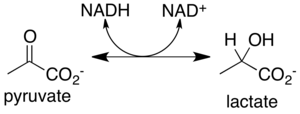
Образование лактата
Пируват, произведенный гликолизом, превращается в лактат. Эта реакция катализированный ферментом лактатдегидрогеназа (LDHA).[1]
пируват + НАДН + Н+ → лактат + НАД+
Образование ацетата
Пируват превращается в ацетил-кофермент А (ацетил-КоА) ферментом пируватдегидрогеназа. Этот ацетил-КоА затем превращается в ацетат в Кишечная палочка, производя АТФ фосфорилирование на уровне субстрата. Для образования ацетата необходимы два фермента: фосфат-ацетилтрансфераза и ацетаткиназа.[1]

ацетил-КоА + фосфат → ацетил-фосфат + КоА
ацетилфосфат + АДФ → ацетат + АТФ
Образование этанола
Этиловый спирт формируется в Кишечная палочка восстановлением ацетилкофермента А с помощью НАДН. Для этой двухступенчатой реакции требуется фермент алкогольдегидрогеназа (ADHE).[1]
ацетил-КоА + НАДН + Н+ → ацетальдегид + НАД+ + CoA
ацетальдегид + НАДН + Н+ → этиловый спирт + НАД+
Формиат образование
Форматировать производится расщепление пирувата. Эта реакция катализируется ферментом пируват-формиатлиаза (PFL), который играет важную роль в регулировании анаэробной ферментации в Кишечная палочка.[7]
пируват + КоА → ацетил-КоА + форматировать
Образование сукцината

Сукцинат формируется в Кишечная палочка в несколько шагов.
Фосфоенолпируват (PEP), путь гликолиза средний, является карбоксилированный ферментом Карбоксилаза PEP формировать оксалоацетат.[8] Затем следует превращение оксалоацетата в малат ферментом малатдегидрогеназа. Фумаратгидратаза затем катализирует дегидратацию малата с образованием фумарат.[9]
фосфоенолпируват + HCO3 → оксалоацетат + фосфат
оксалоацетат + НАДН + Н+ → малат + НАД+
малат → фумарат + H20
Конечная реакция образования сукцината - это восстановление фумарата. Катализируется ферментом фумаратредуктаза.
фумарат + НАДН + Н+ → сукцинат + НАД+
Это снижение является анаэробной реакцией дыхания у Кишечная палочка, поскольку он использует электроны, связанные с НАДН-дегидрогеназой и электронная транспортная цепь. АТФ генерируется с использованием электрохимический градиент и АТФ-синтаза. Это единственный случай в пути смешанной кислотной ферментации, когда АТФ не продуцируется посредством фосфорилирования на уровне субстрата.[1][2]
Витамин К2, также известный как менахинон, очень важен для транспорта электронов к фумарату в Кишечная палочка.[10]
Образование водорода и диоксида углерода
Формиат может быть преобразован в газообразный водород и диоксид углерода в Кишечная палочка. Для этой реакции требуется фермент формиат-водородлиаза. Его можно использовать для предотвращения слишком кислой среды внутри клетки.[1]
форматировать → ЧАС2 и CO2
Метиловый красный тест

В метиловый красный (MR) тест может определить, происходит ли смешанный путь кислотной ферментации у микробов при введении глюкозы. А индикатор pH используется, который окрашивает тестовый раствор в красный цвет, если pH падает ниже 4,4.[11] Если процесс ферментации прошел, полученная смесь кислот сделает раствор очень кислым и вызовет изменение цвета на красный.
Тест на метиловый красный относится к группе, известной как IMViC тесты.
Метаболическая инженерия
Было обнаружено несколько бактериальных штаммов. метаболически сконструированный для увеличения индивидуальных выходов конечных продуктов, образующихся при смешанном кислотном брожении. Например, штаммы для увеличенного производства этанола, лактата, сукцината и ацетата были разработаны из-за полезности этих продуктов в биотехнология.[2] Основным ограничивающим фактором для этой разработки является необходимость поддерживать редокс баланс в смеси кислот, произведенных путем ферментации.[12]
Для производства этанола
Этанол - наиболее часто используемый биотопливо и может производиться в больших масштабах путем ферментации. Максимальный теоретический урожай для производства этанола было достигнуто около 20 лет.[13][14] Плазмида, несущая гены пируватдекарбоксилазы и алкогольдегидрогеназы от бактерий. Z.mobilis использовался учеными. Это было вставлено в Кишечная палочка и привело к увеличению выхода этанола. Геном этого Кишечная палочка штамм KO11 был недавно секвенирован и картирован.[15]


Для производства ацетата
В Кишечная палочка штамм W3110 был генно-инженерный чтобы получить 2 моля ацетата на каждый 1 моль глюкозы, подвергшейся ферментации. Это известно как гомоацетатный путь.[16]
Для производства лактата
Лактат можно использовать для производства биопластик называется Полимолочная кислота (PLA). Свойства PLA зависят от соотношения двух оптические изомеры лактата (D-лактат и L-лактат). D-лактат производится путем смешанной кислотной ферментации в E. coli.[17] В ранних экспериментах был разработан штамм E.coli RR1 для производства одного из двух оптических изомеров лактата.[18]
Более поздние эксперименты модифицировали Штамм E. coli КО11, первоначально разработанный для увеличения производства этанола. Ученые смогли увеличить выход D-лактата от ферментации, выполнив несколько удаления.[19]
Для производства сукцината
Повышение выхода сукцината от смешанной кислотной ферментации впервые было сделано сверхэкспрессия фермент Карбоксилаза PEP.[20] Это давало выход сукцината, который был примерно в 3 раза больше обычного. Было проведено несколько экспериментов с использованием аналогичного подхода.
Альтернативные подходы изменили окислительно-восстановительный потенциал и АТФ баланс для оптимизации выхода сукцината.[21]
Связанные пути ферментации
У микробов есть ряд других путей ферментации.[4] Все эти пути начинаются с преобразования пирувата, но их конечные продукты и ключевые ферменты, которые им необходимы, различны. Эти пути включают:
- Ферментация этанола
- Молочнокислое брожение
- Пропионовая кислота ферментация
- Бутанол ферментация
- Бутандиоловое брожение
внешняя ссылка
Рекомендации
- ^ а б c d е ж грамм час Кеселер, Ингрид М .; и другие. (2011). «EcoCyc: обширная база данных по биологии Escherichia coli». Исследования нуклеиновых кислот. 39 (Проблема с базой данных): D583 – D590. Дои:10.1093 / nar / gkq1143. ЧВК 3013716. PMID 21097882.
- ^ а б c d Фёрстер, Андреас Х. и Йоханнес Гешер (2014). «Метаболическая инженерия Escherichia coli для производства конечных продуктов смешанно-кислотного брожения». Границы биоинженерии и биотехнологии. 2: 506–508. Дои:10.3389 / fbioe.2014.00016. ЧВК 4126452. PMID 25152889.
- ^ М. Магидан и Дж. Мартинко (2006). "Биология микроорганизмов Брока, Нью-Джерси, Пирсон Прентис Холл". 11: 352. Цитировать журнал требует
| журнал =(помощь) - ^ а б Шарма, П. (2007). «Микробиология»: 104. Цитировать журнал требует
| журнал =(помощь) - ^ Фаррелл, Александр Е .; и другие. (2006). «Этанол может способствовать достижению энергетических и экологических целей». Наука. 311 (5760): 506–508. Bibcode:2006Научный ... 311..506F. Дои:10.1126 / science.1121416. PMID 16439656.
- ^ Соерс, Р. Гэри; Блокеш, Мелани; Бёк, август (2004). «Анаэробный формиат и водородный обмен». EcoSal Plus. 1 (1). Дои:10.1128 / ecosalplus.3.5.4. PMID 26443350.
- ^ Кнаппе, Иоахим и Гэри Соэрс (1990). «Радикально-химический путь к ацетил-КоА: анаэробно индуцированная пируватформиат-лиазная система Escherichia coli». Обзор микробиологии FEMS. 6 (4): 383–398. Дои:10.1111 / j.1574-6968.1990.tb04108.x. PMID 2248795.
- ^ Кай, Ясуши, Хироёши Мацумура и Кацура Идзуи (2003). «Фосфоенолпируваткарбоксилаза: трехмерная структура и молекулярные механизмы». Архивы биохимии и биофизики. 414 (2): 170–179. Дои:10.1016 / S0003-9861 (03) 00170-X. PMID 12781768.CS1 maint: несколько имен: список авторов (связь)
- ^ Таккер, Чандреш; и другие. (2012). «Производство сукцината в Escherichia coli». Биотехнологический журнал. 7 (2): 213–224. Дои:10.1002 / biot.201100061. ЧВК 3517001. PMID 21932253.
- ^ Гость, ДЖОН Р. (1977). «Биосинтез менахинона: мутанты Escherichia coli K-12, требующие 2-сукцинилбензоата». Журнал бактериологии. 130 (3): 1038–1046.
- ^ Х. Т. Кларк; У. Р. Кирнер (1922). «Метиловый красный». Орг. Synth. 2: 47. Дои:10.15227 / orgsyn.002.0047.
- ^ ван Хук; Милан Дж. А. и Руланд М. Х. Меркс (2012). «Редокс-баланс является ключом к объяснению полного или частичного перехода на низкоэффективный метаболизм». BMC Systems Biology. 6 (1): 22. Дои:10.1186/1752-0509-6-22. ЧВК 3384451. PMID 22443685.
- ^ Ingram, L.O .; и другие. (1987). «Генная инженерия производства этанола из Escherichia coli». Прикладная и экологическая микробиология. 53:10: 2420–2425.
- ^ Охта, Кадзуёси; и другие. (1991). «Генетическое улучшение Escherichia coli для производства этанола: хромосомная интеграция генов Zymomonas mobilis, кодирующих пируват декарбоксилазу и алкогольдегидрогеназу II». Прикладная и экологическая микробиология. 57 (4): 893–900.
- ^ Тернер, Питер С .; и другие. (2012). «Оптическое картирование и секвенирование генома Escherichia coli KO11 выявляют обширные хромосомные перестройки и множественные тандемные копии генов Zymomonas mobilis pdc и adhB». Журнал промышленной микробиологии и биотехнологии. 39 (4): 629–639. Дои:10.1007 / s10295-011-1052-2. PMID 22075923.
- ^ Causey, T. B .; и другие. (2003). «Разработка метаболизма Escherichia coli W3110 для преобразования сахара в окислительно-восстановительные и окисленные продукты: производство гомоацетата». Труды Национальной академии наук. 100 (3): 825–832. Bibcode:2003ПНАС..100..825С. Дои:10.1073 / pnas.0337684100. ЧВК 298686. PMID 12556564.
- ^ Кларк, Дэвид П. (1989). «Пути ферментации кишечной палочки». Обзор микробиологии FEMS. 5 (3): 223–234. Дои:10.1111 / j.1574-6968.1989.tb03398.x. PMID 2698228.
- ^ Чанг, Донг-Ын; и другие. (1999). «Гомоферментативное производство d-орл-лактата в метаболически сконструированной Escherichia coli RR1». Прикладная и экологическая микробиология. 65 (4): 1384–1389.
- ^ Чжоу, S .; и другие. (2005). «Ферментация 10% (мас. / Об.) Сахара до D (-) - лактата с помощью инженерной Escherichia coli B». Письма о биотехнологии. 27 (23–24): 1891–1896. Дои:10.1007 / s10529-005-3899-7. PMID 16328986.
- ^ Миллард, Синтия Санвилл; и другие. (1996). «Повышенное производство янтарной кислоты за счет сверхэкспрессии фосфоенолпируваткарбоксилазы в Escherichia coli». Прикладная и экологическая микробиология. 62 (5): 1808–1810.
- ^ Сингх, Амарджит; и другие. (2011). «Манипулирование окислительно-восстановительным потенциалом и балансом АТФ для улучшения производства сукцината в E. coli». Метаболическая инженерия. 13 (1): 76–81. Дои:10.1016 / j.ymben.2010.10.006. PMID 21040799.

