Дистилляция - Distillation
Дистилляция это процесс разделение компоненты или вещества из жидкости смесь используя выборочные кипячение и конденсация. Дистилляция может привести к практически полному разделению (почти чистые компоненты), или это может быть частичное разделение, которое увеличивает концентрацию выбранных компонентов в смеси. В любом случае процесс использует различия в относительная волатильность компонентов смеси. В промышленное применение, дистилляция - это работа агрегата практически универсального значения, но это процесс физического разделения, а не химическая реакция.
Дистилляция имеет множество применений. Например:
- Перегонка ферментированный продукция производит дистиллированные напитки с высоким алкоголь содержимое или отделяет другие продукты ферментации, имеющие коммерческую ценность.
- Дистилляция - эффективный и традиционный метод опреснение.
- в нефть промышленность, стабилизация нефти представляет собой форму частичной перегонки, которая снижает давление паров сырой нефти, тем самым делая ее безопасной для хранения и транспортировки, а также сокращая выбросы в атмосферу летучих углеводородов. В промежуточных операциях на нефтеперерабатывающие заводы, фракционная перегонка это основной класс операция для преобразования сырая нефть в топливо и химический сырье.[2][3][4]
- Криогенный дистилляция приводит к разделение воздуха на его компоненты - особенно кислород, азот, и аргон - за промышленное использование.
- в химическая индустрия, большие количества сырых жидких продуктов химический синтез перегоняются для отделения их либо от других продуктов, либо от примесей, либо от непрореагировавших исходных материалов.
Установка, используемая для дистилляции, особенно дистиллированных напитков, - это винокурня. Само дистилляционное оборудование представляет собой Все еще.
История

Ранние свидетельства дистилляции были найдены на Аккадский таблички, датированные c. 1200 г. до н.э. с описанием парфюмерных операций. Таблички содержали текстовые свидетельства того, что ранняя примитивная форма дистилляции была известна Вавилоняне древних Месопотамия.[8] Были также обнаружены ранние свидетельства дистилляции, связанные с алхимики работает в Александрия в Римский Египет в I веке н.э.[9]
Дистиллированная вода используется по крайней мере с. 200 г. н.э., когда Александр Афродисийский описал процесс.[10][11] Работы по перегонке других жидкостей продолжались в начале Византийский Египет под Зосим Панополисский в 3 веке. Дистилляция практиковалась в древние Индийский субконтинент, что видно из обожженной глины возражает и приемники найдены в Таксила, Шайхан Дери, и Чарсадда в современном Пакистан, относящиеся к ранним векам Наша эра.[12][13][14] Эти "Гандхара кадры "были способны производить только очень слабые ликер, так как не было эффективных средств улавливания паров при слабом нагревании.[15]
Дистилляция в Китае, возможно, началась в Восточная Хань династии (1–2 вв. н. э.), но производство напитков началось в Джин (XII – XIII вв.) И Южная Песня (10-13 вв.) Династии, согласно археологическим данным.[16]
Явные доказательства дистилляции алкоголя исходят из Арабский химик Аль-Кинди в 9 веке Ирак,[17][18][19][15] где это было описано Школа Салерно в 12 веке.[9][20] Фракционная перегонка был разработан Тадео Альдеротти в 13 веке.[21] Кадр был найден на археологическом участке в Цинлуне, Хэбэй провинция в Китае, датируемая 12 веком. Дистиллированные напитки были обычным явлением в Династия Юань (13–14 вв.).[16]
В 1500 году немецкий алхимик Иероним Брауншвейг опубликовано Liber de arte destillandi (Книга искусства дистилляции),[22] первая книга, посвященная исключительно теме дистилляции, за ней в 1512 году последовала значительно расширенная версия. В 1651 г. Джон Френч опубликовано Искусство дистилляции,[23] первый крупный английский сборник по практике, но он был востребован[24] в значительной степени это связано с работами Брауншвейга. Сюда входят диаграммы с людьми, показывающими промышленный, а не лабораторный масштаб операции.

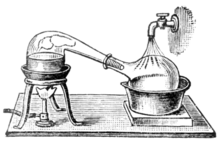


В качестве алхимия превратился в науку о химия, суда назывались возражает стал использоваться для перегонки. Обе перегонные кубы и реплики - это формы изделия из стекла с длинными горлышками, направленными в сторону под углом вниз, чтобы действовать как с воздушным охлаждением конденсаторы к конденсировать дистиллят и дайте ему стечь вниз для сбора. Позже были изобретены медные перегонные кубы. Заклепочные швы часто затягивались с помощью различных смесей, например теста из ржаной муки.[25] Эти перегонные кубы часто имели систему охлаждения вокруг клюва, например, с использованием холодной воды, что делало конденсацию спирта более эффективной. Они назывались горшок. Сегодня реторты и перегонные кубы были в значительной степени вытеснены более эффективными методами дистилляции в большинстве промышленных процессов. Тем не менее, горшок по-прежнему широко используется для производства некоторых прекрасных спиртов, таких как коньяк, Шотландский виски, Ирландский виски, текила, ром, и немного водки. Перегонные кубы из различных материалов (дерево, глина, нержавеющая сталь) также используются в бутлегеры в разных странах. Небольшие перегонные кубы также продаются для использования в отечественном производстве.[26] цветочной воды или эфирные масла.
Ранние формы дистилляции включали периодические процессы с использованием одного испарения и одной конденсации. Чистота была улучшена за счет дальнейшей отгонки конденсата. Большие объемы обрабатывались простым повторением дистилляции. Сообщается, что химики выполнили от 500 до 600 перегонок, чтобы получить чистое соединение.[27]
В начале 19 века основы современных технологий, включая предварительный нагрев и рефлюкс, были разработаны.[27] В 1822 году Энтони Перье разработал один из первых непрерывных перегонных кубов, а затем, в 1826 году, Роберт Штайн улучшил этот дизайн, чтобы сделать свой патент все еще. В 1830 г. Эней Коффи получил патент на дальнейшее улучшение конструкции.[28] Непрерывный перегонный куб Коффи можно рассматривать как архетип современных нефтехимических агрегатов. Французский инженер Арман Саваль разработал свой регулятор пара примерно в 1846 году.[29] В 1877 г. Эрнест Сольвей получил патент США на тарельчатую колонку для аммиак дистилляция[30] и в тот же и последующие годы произошли изменения в этой теме для масел и духов.
С появлением химическая инженерия в качестве дисциплины в конце XIX века можно было применять научные, а не эмпирические методы. Развивающиеся нефть промышленность в начале 20-го века дала толчок к развитию точных методов проектирования, таких как Метод МакКейба – Тиле к Эрнест Тиле и Уравнение Фенске. Первый промышленный завод в Соединенных Штатах, который использовал дистилляцию как средство опреснения океана, открылся в Фрипорт, Техас в 1961 году в надежде принести водная безопасность в регион.[31]Наличие мощных компьютеров позволило напрямую компьютерное моделирование ректификационных колонн.
Применения дистилляции
Применение дистилляции можно условно разделить на четыре группы: лабораторные весы, промышленная перегонка, перегонка трав для парфюмерии и медицины (травяной дистиллят ), и переработка пищевых продуктов. Последние два существенно отличаются от первых двух тем, что дистилляция не используется как истинный метод очистки, а больше для переноса всего летучие вещества от исходного сырья до дистиллята при переработке напитков и трав.
Основное различие между дистилляцией в лабораторном масштабе и промышленной дистилляцией состоит в том, что дистилляция в лабораторном масштабе часто выполняется периодически, тогда как промышленная дистилляция часто происходит непрерывно. В периодическая перегонка, состав исходного материала, пары перегоняемых соединений и дистиллят изменяются во время перегонки. При периодической дистилляции в дистиллятор загружается (поставляется) партия исходной смеси, которая затем разделяется на составляющие фракции, которые собираются последовательно от наиболее летучих к менее летучим, а нижний остаток - остающаяся наименее летучая или нелетучая фракция - удален в конце. После этого можно перезарядить аппарат и повторить процесс.
В непрерывная перегонка исходные материалы, пары и дистиллят поддерживаются в постоянном составе за счет тщательного пополнения исходного материала и удаления фракций как из пара, так и из жидкости в системе. Это приводит к более детальному контролю процесса разделения.
Идеализированная модель дистилляции
В точка кипения жидкости - это температура, при которой давление газа жидкости равняется давлению вокруг жидкости, что позволяет пузырям образовываться без раздавливания. Особый случай - это нормальная точка кипения, где давление пара жидкости равно окружающему атмосферное давление.
Это заблуждение, что в жидкой смеси при заданном давлении каждый компонент кипит при температуре кипения, соответствующей данному давлению, позволяя парам каждого компонента собираться отдельно и в чистом виде. Однако этого не происходит даже в идеализированной системе. Идеализированные модели дистилляции в основном подчиняются Закон Рауля и Закон Дальтона и предположим, что парожидкостное равновесие достигаются.
Закон Рауля гласит, что давление пара в растворе зависит от 1) давления пара каждого химического компонента в растворе и 2) доли раствора, которую составляет каждый компонент, иначе говоря, мольная доля. Этот закон распространяется на идеальные решения или растворы, которые имеют разные компоненты, но молекулярные взаимодействия которых такие же или очень похожи на чистые растворы.
Закон Дальтона гласит, что полное давление - это сумма парциальных давлений каждого отдельного компонента в смеси. Когда многокомпонентная жидкость нагревается, давление пара каждого компонента повышается, что приводит к увеличению общего давления пара. Когда полное давление пара достигает давления, окружающего жидкость, кипячение происходит, и жидкость превращается в газ во всем объеме жидкости. Смесь с заданным составом имеет одну точку кипения при заданном давлении, когда компоненты взаимно растворимы. Смесь постоянного состава не имеет нескольких точек кипения.
Следствием одной точки кипения является то, что более легкие компоненты никогда не «вскипят» чисто. При температуре кипения все летучие компоненты кипят, но для компонента его процентное содержание в паре такое же, как его процент от общего давления пара. Более легкие компоненты имеют более высокое парциальное давление и, таким образом, концентрируются в паре, но более тяжелые летучие компоненты также имеют (меньшее) парциальное давление и обязательно также испаряются, хотя и при более низкой концентрации в паре. Действительно, периодическая дистилляция и фракционирование достигаются за счет изменения состава смеси. При периодической перегонке партия испаряется, что меняет ее состав; при фракционировании жидкость выше в колонне фракционирования содержит больше легкого и кипит при более низких температурах. Следовательно, исходя из данной смеси, кажется, что она имеет интервал кипения, а не точку кипения, хотя это происходит потому, что ее состав изменяется: каждая промежуточная смесь имеет свою собственную особую точку кипения.
Идеализированная модель точна в случае химически подобных жидкостей, таких как бензол и толуол. В других случаях наблюдаются серьезные отклонения от закона Рауля и закона Дальтона, наиболее известные из них в смеси этанола и воды. Эти соединения при совместном нагревании образуют азеотроп, когда паровая фаза и жидкая фаза содержат один и тот же состав. Хотя есть вычислительные методы который можно использовать для оценки поведения смеси произвольных компонентов, единственный способ получить точные парожидкостное равновесие данные получены путем измерения.
Невозможно полностью очистить смесь компонентов дистилляцией, так как это потребует, чтобы каждый компонент в смеси имел нулевое значение. частичное давление. Если целью являются сверхчистые продукты, то дальше химическое разделение должны применяться. Когда бинарная смесь испаряется, а другой компонент, например соль, имеет нулевое парциальное давление для практических целей, процесс проще.
Периодическая или дифференциальная дистилляция
Нагревание идеальной смеси двух летучих веществ, A и B, с A, имеющим более высокую летучесть или более низкую температуру кипения, в установке периодической дистилляции (например, в устройстве, изображенном на начальном рисунке) до кипения смеси приводит к пар над жидкостью, который содержит смесь A и B. Соотношение между A и B в паре будет отличаться от соотношения в жидкости. Соотношение в жидкости будет определяться тем, как была приготовлена исходная смесь, в то время как соотношение в паре будет обогащено более летучим соединением А (согласно закону Рауля, см. Выше). Пар проходит через конденсатор и удаляется из системы. Это, в свою очередь, означает, что соотношение соединений в оставшейся жидкости теперь отличается от начального соотношения (то есть более обогащено B, чем в исходной жидкости).
В результате соотношение в жидкой смеси изменяется, становясь богаче компонентом B. Это вызывает повышение температуры кипения смеси, что приводит к повышению температуры пара, что приводит к изменению отношения A : B в газовой фазе (по мере продолжения дистилляции доля B в газовой фазе увеличивается). Это приводит к медленному изменению соотношения A: B в дистилляте.
Если разница в давлении паров между двумя компонентами A и B велика - обычно выражается как разница в точках кипения - смесь в начале перегонки сильно обогащена компонентом A, а когда компонент A отгоняется, кипящая жидкость обогащена компонентом Б.
Непрерывная перегонка
Непрерывная перегонка - это непрерывная перегонка, при которой жидкая смесь непрерывно (без перерыва) подается в процесс, а разделенные фракции непрерывно удаляются, поскольку потоки на выходе возникают с течением времени во время операции. Непрерывная перегонка дает минимум две фракции на выходе, включая как минимум одну летучий фракция дистиллята, которая закипела и была отдельно захвачена в виде пара, а затем конденсирована в жидкость. Всегда существует нижняя (или остаточная) фракция, которая представляет собой наименее летучий остаток, который не улавливался отдельно в виде конденсированного пара.
Непрерывная дистилляция отличается от периодической дистилляции тем, что концентрации не должны изменяться с течением времени. Непрерывная перегонка может выполняться при устойчивое состояние на произвольный промежуток времени. Для любого исходного материала определенного состава основными переменными, влияющими на чистоту продуктов при непрерывной перегонке, являются коэффициент дефлегмации и количество теоретических ступеней равновесия, которые на практике определяются количеством тарелок или высотой насадки. Обратный поток - это поток из конденсатора обратно в колонку, который создает рециркуляцию, которая позволяет лучше разделить с заданным количеством тарелок. Стадии равновесия являются идеальными стадиями, на которых композиции достигают равновесия пар-жидкость, повторяя процесс разделения и обеспечивая лучшее разделение с учетом коэффициента орошения. Колонна с высоким коэффициентом орошения может иметь меньше ступеней, но она пропускает большое количество жидкости, образуя широкую колонну с большой задержкой. И наоборот, колонна с низким коэффициентом флегмы должна иметь большое количество ступеней, что требует более высокой колонны.
Общие улучшения
Как периодическую, так и непрерывную дистилляцию можно улучшить, используя колонна фракционирования сверху перегонной колбы. Колонна улучшает разделение, обеспечивая большую площадь поверхности для соприкосновения пара и конденсата. Это помогает ему оставаться в равновесии как можно дольше. Колонна может даже состоять из небольших подсистем («тарелок» или «тарелок»), каждая из которых содержит обогащенную кипящую жидкую смесь, каждая из которых имеет собственное парожидкостное равновесие.
Между фракционирующими колоннами лабораторного и промышленного масштаба есть различия, но принципы те же. Примеры фракционирующих колонн лабораторного масштаба (для повышения эффективности) включают:
- Конденсатор воздуха
- Колонна Вигре (обычно только в лабораторных масштабах)
- Насадочная колонна (упакованы стеклянными шариками, металлическими деталями или другим химически инертным материалом)
- Прядильная перегонка система.
Лабораторная дистилляция
Дистилляции в лабораторных масштабах почти всегда проводятся как периодические. Устройство, используемое при дистилляции, иногда называют Все еще, состоит как минимум из ребойлер или же горшок в котором исходный материал нагревается, конденсатор в котором нагревается пар охлаждается обратно в жидкость государственный, а приемник в котором концентрированная или очищенная жидкость, называемая дистиллят, собрано. Существует несколько лабораторных методов перегонки (см. Также виды дистилляции).
Полностью герметичный дистилляционный аппарат может испытывать чрезмерное и быстро меняющееся внутреннее давление, что может привести к его разрыву в местах соединения. Поэтому какой-то путь обычно оставляют открытым (например, у приемной колбы), чтобы позволить внутреннему давлению уравняться с атмосферным давлением. В качестве альтернативы вакуумный насос может использоваться для поддержания давления в аппарате ниже атмосферного. Если задействованные вещества чувствительны к воздуху или влаге, связь с атмосферой может осуществляться через один или несколько сушильные трубы упакованы материалами, удаляющими нежелательные компоненты воздуха, или барботеры которые обеспечивают подвижный барьер для жидкости. Наконец, попадание нежелательных компонентов воздуха можно предотвратить, закачивая слабый, но постоянный поток подходящего инертного газа, например азот, в аппарат.
Простая перегонка
В простая перегонка, пар сразу же направляется в конденсатор. Следовательно, дистиллят не является чистым, а его состав идентичен составу паров при данной температуре и давлении. Эта концентрация следует за Закон Рауля.
В результате простая перегонка эффективна только тогда, когда точки кипения жидкости сильно различаются (практическое правило - 25 ° C).[32] или при отделении жидкостей от нелетучих твердых веществ или масел. В этих случаях давления пара компонентов обычно достаточно различаются, чтобы дистиллят мог быть достаточно чистым для его предполагаемого назначения.
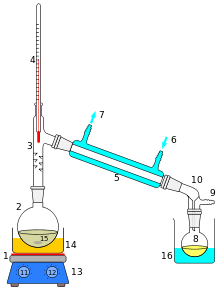
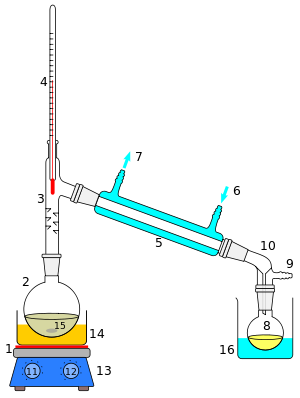
Краткое схематическое изображение простой операции дистилляции показано слева. Стартовая жидкость 15 в кипящей колбе 2 отапливается комбинированным горячая тарелка и магнитная мешалка 13 через силиконовое масло ванна (апельсин, 14). Пар проходит через короткую Колонна Вигре 3, затем через Конденсатор Либиха 5, охлаждается водой (синий цвет), которая циркулирует через порты 6 и 7. Конденсированная жидкость капает в приемную колбу. 8, сидя в охлаждающей ванне (синий, 16). Адаптер 10 имеет связь 9 который может быть установлен на вакуумный насос. Компоненты соединены между собой стыки матового стекла (серый).
Фракционная перегонка

Во многих случаях точки кипения компонентов смеси будут достаточно близкими, чтобы Закон Рауля необходимо принять во внимание. Следовательно, фракционная перегонка должны использоваться для разделения компонентов с помощью повторяющихся циклов испарения-конденсации в насадочной ректификационной колонне. Это разделение путем последовательных перегонок также называется исправление.[33]
При нагревании очищаемого раствора его пары поднимаются до колонна фракционирования. Поднимаясь, он охлаждается, конденсируясь на стенках конденсатора и поверхностях упаковочного материала. Здесь конденсат продолжает нагреваться поднимающимися горячими парами; он снова испаряется. Однако состав свежих паров снова определяется законом Рауля. Каждый цикл испарения-конденсации (называемый теоретическая тарелка ) даст более чистый раствор более летучего компонента.[34] В действительности, каждый цикл при данной температуре не происходит точно в одном и том же месте фракционирующей колонны; теоретическая тарелка таким образом, это скорее концепция, чем точное описание.
Чем больше теоретических тарелок, тем лучше разделение. А прядильная ленточная перегонка система использует вращающуюся ленту Тефлон или металл, чтобы заставить поднимающиеся пары плотно контактировать с нисходящим конденсатом, увеличивая количество теоретических тарелок.[35]
Паровая дистилляция
Нравиться вакуумная перегонка, паровая дистилляция это метод перегонки термочувствительных веществ.[36] Температуру пара легче контролировать, чем температуру поверхности нагревательный элемент, и обеспечивает высокую скорость передачи тепла без нагрева при очень высокой температуре. Этот процесс включает в себя пропускание пара через нагретую смесь сырья. По закону Рауля часть целевого соединения будет испаряться (в соответствии с его парциальным давлением). Смесь паров охлаждается и конденсируется, обычно образуя слой масла и слой воды.
Паровая перегонка различных ароматный травы и цветы могут дать два продукта; ан Эфирное масло а также водянистый травяной дистиллят. В эфирные масла часто используются в парфюмерии и ароматерапия в то время как водянистые дистилляты находят множество применений в ароматерапия, переработка пищевых продуктов и ухаживать за кожей.


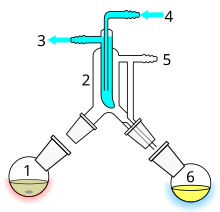
1: Мешалка / гранулы, предотвращающие удары 2: Еще горшок 3: Колонна фракционирования 4: Термометр / Температура кипения 5: Тефлоновый кран 1 6: Холодный палец 7: Выход охлаждающей воды 8: Охлаждающая вода в 9: Тефлоновый кран 2 10: Вход вакуума / газа 11: Тефлоновый кран 3 12: Еще приемник
Вакуумная перегонка
Некоторые соединения имеют очень высокую температуру кипения. Для кипячения таких соединений часто лучше снизить давление, при котором они кипятятся, а не повышать температуру. Как только давление понижается до давления пара соединения (при данной температуре), можно начинать кипение и остальную часть процесса дистилляции. Этот метод упоминается как вакуумная перегонка и его обычно находят в лаборатории в виде роторный испаритель.
Этот метод также очень полезен для соединений, температура кипения которых превышает их Температура разложения при атмосферном давлении и, следовательно, разложились бы при любой попытке кипячения при атмосферном давлении.
Молекулярная дистилляция - вакуумная перегонка ниже давления 0,01 торр. 0,01 торр на порядок выше высокий вакуум, где жидкости находятся в свободный молекулярный поток режим, т.е. длина свободного пробега молекул сопоставимо с размером оборудования. Газовая фаза больше не оказывает значительного давления на испаряемое вещество, и, следовательно, скорость испарения больше не зависит от давления. То есть, поскольку континуальные предположения гидродинамики больше не применимы, массоперенос определяется молекулярной динамикой, а не гидродинамикой. Таким образом, необходим короткий путь между горячей поверхностью и холодной поверхностью, обычно путем подвешивания горячей пластины, покрытой пленкой корма, рядом с холодной пластиной с прямой видимостью между ними. Молекулярная дистилляция используется в промышленности для очистки масел.
Воздухочувствительная вакуумная перегонка
Некоторые соединения имеют высокие температуры кипения, а также чувствительный к воздуху. Можно использовать простую систему вакуумной дистилляции, как проиллюстрировано выше, в которой вакуум заменяется инертным газом после завершения дистилляции. Однако это менее удовлетворительная система, если кто-то хочет собирать фракции при пониженном давлении. Для этого к концу конденсатора можно добавить адаптер «корова» или «свинья», или для лучших результатов или для очень чувствительных к воздуху соединений Треугольник Перкина аппарат можно использовать.
Треугольник Перкина имеет средства через серию стеклянных или Тефлон отводы, позволяющие изолировать фракции от остальной части Все еще, без удаления основной части дистилляции из вакуума или источника тепла, и, таким образом, может оставаться в состоянии рефлюкс. Для этого образец сначала изолируется от вакуума с помощью кранов, затем вакуум над образцом заменяется инертным газом (например, азот или же аргон ), а затем его можно закрыть пробкой и удалить. Затем в систему можно добавить свежий сборный сосуд, откачать его и снова подключить к дистилляционной системе через краны для сбора второй фракции и так далее, пока не будут собраны все фракции.
Дистилляция по короткому пути
Дистилляция по короткому пути это метод перегонки, при котором дистиллят перемещается на небольшое расстояние, часто всего несколько сантиметров, и обычно проводится при пониженном давлении.[37] Классическим примером может служить перегонка, при которой дистиллят перемещается из одной стеклянной колбы в другую, без необходимости использования конденсатора, разделяющего две камеры. Этот метод часто используется для соединений, которые нестабильны при высоких температурах, или для очистки небольших количеств соединения. Преимущество состоит в том, что температура нагрева может быть значительно ниже (при пониженном давлении), чем точка кипения жидкости при стандартном давлении, и дистиллят должен пройти лишь небольшое расстояние до конденсации. Короткий путь гарантирует, что небольшое количество компаунда теряется по бокам устройства. В Kugelrohr представляет собой своего рода перегонный аппарат с коротким ходом, который часто содержит несколько камер для сбора фракций дистиллята.
Зонная дистилляция
Зонная перегонка - это процесс перегонки в длинном контейнере с частичным плавлением очищенного вещества в зоне движущейся жидкости и конденсацией пара в твердой фазе при отводе конденсата в холодной зоне. Процесс проработан теоретически. При перемещении зонного нагревателя от верха к низу емкости образуется твердый конденсат с неравномерным распределением примесей. Тогда наиболее чистая часть конденсата может быть извлечена как продукт. Процесс можно многократно повторять, перемещая (без оборота) полученный конденсат в нижнюю часть емкости на место очищенного вещества. Неравномерное распределение примесей в конденсате (то есть эффективность очистки) увеличивается с количеством итераций. Зональная дистилляция является дистилляционным аналогом зонной перекристаллизации. Распределение примесей в конденсате описывается известными уравнениями зонной перекристаллизации - с заменой коэффициента распределения k кристаллизации на коэффициент разделения дистилляции α.[38][39][40]
Другие типы
- Процесс реактивная перегонка предполагает использование реакционного сосуда в качестве перегонного куба. В этом процессе продукт обычно имеет значительно более низкую температуру кипения, чем его реагенты. Поскольку продукт образуется из реагентов, он испаряется и удаляется из реакционной смеси. Этот метод является примером непрерывного против периодического процесса; Преимущества включают меньшее время простоя для загрузки реакционного сосуда исходным материалом и меньшую переработку. Дистилляцию «над реагентом» можно классифицировать как реактивную дистилляцию. Обычно он используется для удаления летучих примесей из дистилляционного сырья. Например, немного Лайм может быть добавлен для удаления диоксида углерода из воды с последующей второй дистилляцией с небольшим серная кислота добавлен для удаления следов аммиака.
- Каталитическая перегонка это процесс, с помощью которого реагенты катализируются во время перегонки для непрерывного отделения продуктов от реагентов. Этот метод используется, чтобы способствовать завершению равновесных реакций.
- Первапорация представляет собой метод разделения смесей жидкостей путем частичного испарения через непористый мембрана.
- Экстракционная перегонка определяется как перегонка в присутствии смешивающегося, высококипящего, относительно нелетучего компонента, растворителя, который не образует азеотроп с другими компонентами смеси.
- Мгновенное испарение (или частичное испарение) - это частичное испарение что происходит, когда поток насыщенной жидкости подвергается снижению давления, проходя через дросселирование клапан или другое дросселирующее устройство. Этот процесс - одна из простейших единичных операций, эквивалентная дистилляции с одной стадией равновесия.
- Кодистилляция - это дистилляция, которая выполняется для смесей, в которых два соединения не смешиваются. В лаборатории Аппарат Дина-Старка для этого используется для удаления воды из продуктов синтеза. Bleidner - еще один пример с двумя кипящими растворителями.
- Мембранная перегонка - это тип перегонки, при котором пары разделяемой смеси проходят через мембрану, которая избирательно проникает в один компонент смеси. Движущей силой является перепад давления пара. Он имеет потенциальное применение при опреснении морской воды и удалении органических и неорганических компонентов.
Единичный процесс испарение также может называться «дистилляция»:
- В роторное испарение аппарат вакуумной перегонки используется для удаления сыпучих материалов растворители по образцу. Обычно вакуум создается аспиратор воды или мембранный насос.
- В Kugelrohr обычно используется короткокипящий перегонный аппарат (обычно в сочетании с (высоким) вакуумом) для перегонки высококипящих (> 300 ° C) соединений. Устройство состоит из печи, в которую помещают перегоняемое соединение, приемной части, которая находится вне печи, и средства вращения образца. Вакуум обычно создается с помощью высоковакуумного насоса.
Другое использование:
- Сухая перегонка или же деструктивная перегонка, несмотря на название, на самом деле это не дистилляция, а скорее химическая реакция известный как пиролиз в котором твердые вещества нагреваются в инертном или сокращение улавливают атмосферу и любые летучие фракции, содержащие высококипящие жидкости и продукты пиролиза. Разрушительная перегонка дерево давать метанол это корень его общего имени - древесный спирт.
- Замораживание дистилляции аналогичный метод очистки с использованием замораживание вместо испарения. Это не настоящая дистилляция, а перекристаллизация где продукт маточный раствор, и не производит продуктов, эквивалентных дистилляции. Этот процесс используется при производстве ледяное пиво и ледяное вино для увеличения этанола и сахар content соответственно. Он также используется для производства Эпплджек. В отличие от дистилляции, дистилляция с замораживанием концентрирует ядовитые родственные соединения, а не удаляет их; В результате многие страны запрещают такую яблочную джек в качестве меры здоровья. Кроме того, их можно разделить перегонкой путем выпаривания, поскольку они имеют разные точки кипения.
Азеотропная перегонка
Взаимодействие между компонентами раствора создает свойства, уникальные для раствора, поскольку большинство процессов влечет за собой неидеальные смеси, где Закон Рауля не держит. Такое взаимодействие может привести к постоянному кипению. азеотроп который ведет себя так, как если бы это было чистое соединение (то есть кипит при одной температуре, а не при диапазоне). При азеотропе раствор содержит данный компонент в той же пропорции, что и пар, так что испарение не влияет на чистоту, а дистилляция не влияет на разделение. Например, этиловый спирт и воды образуют 95,6% азеотроп при 78,1 ° C.
Если азеотроп не считается достаточно чистым для использования, существуют некоторые методы разрушения азеотропа с получением чистого дистиллята. Этот набор методов известен как азеотропная дистилляция. Некоторые методы достигают этого путем «перепрыгивания» над азеотропной композицией (путем добавления другого компонента для создания нового азеотропа или путем изменения давления). Другие работают путем химического или физического удаления или изоляции примесей. Например, чтобы очистить этанол более 95%, осушающий агент (или осушитель, Такие как карбонат калия ) может быть добавлен для превращения растворимой воды в нерастворимую кристаллизационная вода. Молекулярные сита также часто используются для этой цели.
Несмешивающиеся жидкости, такие как вода и толуол, легко образуют азеотропы. Обычно эти азеотропы называют низкокипящими азеотропами, потому что температура кипения азеотропа ниже, чем точка кипения любого из чистых компонентов. Температуру и состав азеотропа легко предсказать по давлению паров чистых компонентов без использования закона Рауля. Азеотроп легко разрушается в дистилляционной установке, используя сепаратор жидкость-жидкость (декантатор) для разделения двух жидких слоев, которые конденсируются наверху. Только один из двух жидких слоев нагнетается в дистилляционную установку.
Также существуют азеотропы с высокой температурой кипения, такие как смесь соляной кислоты с водой на 20% по весу. As implied by the name, the boiling point of the azeotrope is greater than the boiling point of either pure component.
To break azeotropic distillations and cross distillation boundaries, such as in the DeRosier Problem, it is necessary to increase the composition of the light key in the distillate.
Breaking an azeotrope with unidirectional pressure manipulation
The boiling points of components in an azeotrope overlap to form a band. By exposing an azeotrope to a vacuum or positive pressure, it's possible to bias the boiling point of one component away from the other by exploiting the differing vapor pressure curves of each; the curves may overlap at the azeotropic point, but are unlikely to be remain identical further along the pressure axis either side of the azeotropic point. When the bias is great enough, the two boiling points no longer overlap and so the azeotropic band disappears.
This method can remove the need to add other chemicals to a distillation, but it has two potential drawbacks.
Under negative pressure, power for a vacuum source is needed and the reduced boiling points of the distillates requires that the condenser be run cooler to prevent distillate vapors being lost to the vacuum source. Increased cooling demands will often require additional energy and possibly new equipment or a change of coolant.
Alternatively, if positive pressures are required, standard glassware can not be used, energy must be used for pressurization and there is a higher chance of side reactions occurring in the distillation, such as decomposition, due to the higher temperatures required to effect boiling.
A unidirectional distillation will rely on a pressure change in one direction, either positive or negative.
Pressure-swing distillation
Pressure-swing distillation is essentially the same as the unidirectional distillation used to break azeotropic mixtures, but here both positive and negative pressures may be employed.
This improves the selectivity of the distillation and allows a chemist to optimize distillation by avoiding extremes of pressure and temperature that waste energy. This is particularly important in commercial applications.
One example of the application of pressure-swing distillation is during the industrial purification of ethyl acetate after its catalytic synthesis from этиловый спирт.
Industrial distillation

Large scale industrial distillation applications include both batch and continuous fractional, vacuum, azeotropic, extractive, and steam distillation. The most widely used industrial applications of continuous, steady-state fractional distillation are in petroleum refineries, нефтехимический и химические заводы и переработка природного газа растения.
To control and optimize such industrial distillation, a standardized laboratory method, ASTM D86, is established. This test method extends to the atmospheric distillation of petroleum products using a laboratory batch distillation unit to quantitatively determine the boiling range characteristics of petroleum products.
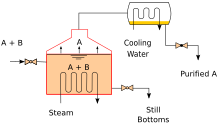
Industrial distillation[33][41] is typically performed in large, vertical cylindrical columns known as distillation towers или же distillation columns with diameters ranging from about 65 centimeters to 16 meters and heights ranging from about 6 meters to 90 meters or more. When the process feed has a diverse composition, as in distilling сырая нефть, liquid outlets at intervals up the column allow for the withdrawal of different фракции or products having different точки кипения or boiling ranges. The "lightest" products (those with the lowest boiling point) exit from the top of the columns and the "heaviest" products (those with the highest boiling point) exit from the bottom of the column and are often called the bottoms.
Industrial towers use рефлюкс to achieve a more complete separation of products. Reflux refers to the portion of the condensed overhead liquid product from a distillation or fractionation tower that is returned to the upper part of the tower as shown in the schematic diagram of a typical, large-scale industrial distillation tower. Inside the tower, the downflowing reflux liquid provides cooling and condensation of the upflowing vapors thereby increasing the efficiency of the distillation tower. The more reflux that is provided for a given number of теоретические тарелки, the better the tower's separation of lower boiling materials from higher boiling materials. Alternatively, the more reflux that is provided for a given desired separation, the fewer the number of theoretical plates required. Инженеры-химики must choose what combination of reflux rate and number of plates is both economically and physically feasible for the products purified in the distillation column.
Such industrial fractionating towers are also used in криогенный разделение воздуха, производя жидкий кислород, жидкий азот, and high purity аргон. Distillation of chlorosilanes also enables the production of high-purity кремний для использования в качестве полупроводник.
Design and operation of a distillation tower depends on the feed and desired products. Given a simple, binary component feed, analytical methods such as the McCabe–Thiele method[33][42] или Fenske equation[33] может быть использован. For a multi-component feed, симуляция models are used both for design and operation. Moreover, the efficiencies of the vapor–liquid contact devices (referred to as "plates" or "trays") used in distillation towers are typically lower than that of a theoretical 100% efficient equilibrium stage. Hence, a distillation tower needs more trays than the number of theoretical vapor–liquid equilibrium stages. A variety of models have been postulated to estimate tray efficiencies.
In modern industrial uses, a packing material is used in the column instead of trays when low pressure drops across the column are required. Other factors that favor packing are: vacuum systems, smaller diameter columns, corrosive systems, systems prone to foaming, systems requiring low liquid holdup, and batch distillation. Conversely, factors that favor plate columns are: presence of solids in feed, high liquid rates, large column diameters, complex columns, columns with wide feed composition variation, columns with a chemical reaction, absorption columns, columns limited by foundation weight tolerance, low liquid rate, large turn-down ratio and those processes subject to process surges.

This packing material can either be random dumped packing (1–3" wide) such as Кольца Рашига или же structured sheet metal. Liquids tend to wet the surface of the packing and the vapors pass across this wetted surface, where массообмен происходит. Unlike conventional tray distillation in which every tray represents a separate point of vapor–liquid equilibrium, the vapor–liquid equilibrium curve in a packed column is continuous. However, when modeling packed columns, it is useful to compute a number of "theoretical stages" to denote the separation efficiency of the packed column with respect to more traditional trays. Differently shaped packings have different surface areas and void space between packings. Оба эти фактора влияют на характеристики набивки.
Another factor in addition to the packing shape and surface area that affects the performance of random or structured packing is the liquid and vapor distribution entering the packed bed. Количество теоретические этапы необходимое для данного разделения рассчитывается с использованием определенного отношения пара к жидкости. If the liquid and vapor are not evenly distributed across the superficial tower area as it enters the packed bed, the liquid to vapor ratio will not be correct in the packed bed and the required separation will not be achieved. Кажется, что упаковка работает неправильно. В высота эквивалентна теоретической тарелке (HETP) будет больше, чем ожидалось. Проблема не в самой насадке, а в неправильном распределении жидкостей, поступающих в насадочный слой. Liquid mal-distribution is more frequently the problem than vapor. The design of the liquid distributors used to introduce the feed and reflux to a packed bed is critical to making the packing perform to it maximum efficiency. Methods of evaluating the effectiveness of a liquid distributor to evenly distribute the liquid entering a packed bed can be found in references.[44][45] Considerable work has been done on this topic by Fractionation Research, Inc. (commonly known as FRI).[46]
Multi-effect distillation
The goal of multi-effect distillation is to increase the energy efficiency of the process, for use in desalination, or in some cases one stage in the production of ultrapure water. The number of effects is inversely proportional to the kW·h/m3 of water recovered figure, and refers to the volume of water recovered per unit of energy compared with single-effect distillation. One effect is roughly 636 kW·h/m3.
- Multi-stage flash distillation can achieve more than 20 effects with thermal energy input, as mentioned in the article.
- Vapor compression evaporation – Commercial large-scale units can achieve around 72 effects with electrical energy input, according to manufacturers.
There are many other types of multi-effect distillation processes, including one referred to as simply multi-effect distillation (MED), in which multiple chambers, with intervening heat exchangers, are employed.
Distillation in food processing
Дистиллированные напитки
Углеводы -containing plant materials are allowed to ferment, producing a dilute solution of ethanol in the process. Spirits such as виски и ром are prepared by distilling these dilute solutions of ethanol. Components other than ethanol, including water, esters, and other alcohols, are collected in the condensate, which account for the flavor of the beverage. Some of these beverages are then stored in barrels or other containers to acquire more flavor compounds and characteristic flavors.
Галерея
 | Chemistry in its beginnings used retorts в качестве Лабораторное оборудование exclusively for distillation processes. |
 | A simple set-up to distill dry and oxygen-free толуол. |
 | Diagram of an industrial-scale vacuum distillation column as commonly used in нефтеперерабатывающие заводы |
 | А rotary evaporator is able to distill solvents more quickly at lower temperatures through the use of a вакуум. |
 | Distillation using semi-microscale apparatus. The jointless design eliminates the need to fit pieces together. The pear-shaped flask allows the last drop of residue to be removed, compared with a similarly-sized круглодонная колба The small holdup volume prevents losses. A pig is used to channel the various distillates into three receiving flasks. If necessary the distillation can be carried out under vacuum using the vacuum adapter at the pig. |
Смотрите также
- Атмосферная перегонка сырой нефти
- Clyssus
- Fragrance extraction
- Микродистиллерий
- Sublimation
- Кольца Диксона
- Случайная упаковка колонок
Рекомендации
- ^ Harwood & Moody 1989, стр. 141–143
- ^ Schaschke, C., 2014. A Dictionary of Chemical Engineering. Издательство Оксфордского университета.
- ^ 2019. Distillation: The Historical Symbol of Chemical Engineering. The University of Toledo. URL https://www.utoledo.edu/engineering/chemical-engineering/distillation.html
- ^ 2017. Products made from petroleum. Ranken Energy Corporation. URL https://www.ranken-energy.com/index.php/products-made-from-petroleum/
- ^ Gildemeister, E.; Hoffman, Fr.; translated by Edward Kremers (1913). The Volatile Oils. 1. Нью-Йорк: Вили. п. 203.
- ^ Bryan H. Bunch; Alexander Hellemans (2004). The History of Science and Technology. Houghton Mifflin Harcourt. п.88. ISBN 978-0-618-22123-3.
- ^ Berthelot, Marcelin (1887–1888) Collection des anciens alchimistes grecs. 3 vol., Paris, p. 161
- ^ Levey, Martin (1959). Chemistry and Chemical Technology in Ancient Mesopotamia. Эльзевир. п. 36.
As already mentioned, the textual evidence for Sumero-Babylonian distillation is disclosed in a group of Akkadian tablets describing perfumery operations, dated ca. 1200 B.C.
- ^ а б Forbes 1970, pp. 57, 89
- ^ Taylor, F. (1945). "The evolution of the still". Анналы науки. 5 (3): 185. Дои:10.1080/00033794500201451.
- ^ Berthelot, M. P. E. M. (1893). "The Discovery of Alcohol and Distillation". The Popular Science Monthly. XLIII: 85–94. В архиве с оригинала от 29 ноября 2017 г.
- ^ Джон Маршалл, Таксила, 2:420, 1951
- ^ Frank Raymond Allchin, "India: the ancient home of distillation?" мужчина, Новая серия 14:1:55-63 (1979) полный текст
- ^ Javed Husain, "The So-Called 'Distillery' at Shaikhan Dheri - A Case Study", Журнал Пакистанского исторического общества 41:3:289-314 (Jul 1, 1993)
- ^ а б Habib, Irfan (2011), Economic History of Medieval India, 1200–1500. Pearson Education. п. 55. ISBN 9788131727911
- ^ а б Haw, Stephen G. (2012). "Wine, women and poison". Marco Polo in China. Рутледж. С. 147–148. ISBN 978-1-134-27542-7.
The earliest possible period seems to be the Eastern Han dynasty ... the most likely period for the beginning of true distillation of spirits for drinking in China is during the Jin and Southern Song dynasties
- ^ аль-Хасан, Ахмад Й. (2001), Science and Technology in Islam: Technology and applied sciences. ЮНЕСКО. С. 65–69. ISBN 9789231038310
- ^ Hassan, Ahmad Y. "Alcohol and the Distillation of Wine in Arabic Sources". История науки и техники в исламе. В архиве from the original on 29 December 2015. Получено 19 апреля 2014.
- ^ The Economist: "Liquid fire – The Arabs discovered how to distil alcohol. They still do it best, say some" В архиве 22 October 2012 at the Wayback Machine December 18, 2003
- ^ Sarton, George (1975). Introduction to the history of science. R. E. Krieger Pub. Co. p. 145. ISBN 978-0-88275-172-6.
- ^ Holmyard, Eric John (1990). Алхимия. Courier Dover Publications. п.53. ISBN 978-0-486-26298-7.
- ^ Braunschweig, Hieronymus (1500). Liber de arte destillandi, de Simplicibus [The Book of the Art of Distillation] (на немецком).
- ^ French, John (1651). The Art of Distillation. London: Richard Cotes.
- ^ "Distillation". Промышленная и инженерная химия. 28 (6): 677. 1936. Дои:10.1021/ie50318a015.
- ^ Sealing Technique, accessed 16 November 2006.
- ^ Traditional Alembic Pot Still В архиве 21 November 2006 at the Wayback Machine, accessed 16 November 2006.
- ^ а б Othmer, D. F. (1982) "Distillation – Some Steps in its Development", in W. F. Furter (ed) A Century of Chemical Engineering. ISBN 0-306-40895-3
- ^ GB 5974, Coffey, A., "Apparatus for Brewing and Distilling", published 5 August 1830, issued 5 February 1831; изображение В архиве 4 февраля 2017 г. Wayback Machine
- ^ Forbes 1970, п. 323
- ^ US 198699, Solvay, Ernest, "Improvement in the Ammonia-Soda Manufacture", published 2 June 1876, issued 25 December 1877
- ^ "Making the Deserts Bloom: Harnessing nature to deliver us from drought, Distillations Podcast and transcript, Episode 239". Институт истории науки. 19 марта 2019 г.. Получено 27 августа 2019.
- ^ ST07 Separation of liquid–liquid mixtures (solutions), DIDAC by ИЮПАК
- ^ а б c d Perry, Robert H.; Green, Don W. (1984). Справочник инженеров-химиков Перри (6-е изд.). Макгроу-Хилл. ISBN 978-0-07-049479-4.
- ^ Fractional Distillation. fandm.edu
- ^ Spinning Band Distillation В архиве 25 августа 2006 г. Wayback Machine. B/R Instrument Corporation (accessed 8 September 2006)
- ^ Harwood & Moody 1989, pp. 151–153
- ^ Harwood & Moody 1989, п. 150
- ^ Kravchenko, A. I. (2011). "Зонная дистилляция: новый метод рафинирования" [Zone distillation: a new method of refining]. Problems of Atomic Science and Technology (на русском). 6 (19): 24–26.
- ^ Kravchenko, A. I. (2014). "Zone distillation: justification". Problems of Atomic Science and Technology. 1 (20): 64–65.
- ^ Kravchenko, A. I. (2014). "Разработка перспективных схем зонной дистилляции" [Design of advanced processes of zone distillation]. Perspectivnye Materialy (in Russian) (7): 68–72.
- ^ Кистер, Генри З. (1992). Дизайн дистилляции (1-е изд.). Макгроу-Хилл. ISBN 978-0-07-034909-4.
- ^ Seader, J. D.; Henley, Ernest J. (1998). Принципы процесса разделения. Нью-Йорк: Вили. ISBN 978-0-471-58626-5.
- ^ Energy Institute website page В архиве 12 октября 2007 г. Wayback Machine. Resources.schoolscience.co.uk. Retrieved on 2014-04-20.
- ^ Moore, F., Rukovena, F. (August 1987) Random Packing, Vapor and Liquid Distribution: Liquid and gas distribution in commercial packed towers, Chemical Plants & Processing, Edition Europe, pp. 11–15
- ^ Spiegel, L (2006). "A new method to assess liquid distributor quality". Chemical Engineering and Processing. 45 (11): 1011. Дои:10.1016/j.cep.2006.05.003.
- ^ Kunesh, John G.; Lahm, Lawrence; Yanagi, Takashi (1987). "Commercial scale experiments that provide insight on packed tower distributors". Industrial & Engineering Chemistry Research. 26 (9): 1845. Дои:10.1021/ie00069a021.
Цитированные источники
- Forbes, R. J. (1970). A Short History of the Art of Distillation from the Beginnings up to the Death of Cellier Blumenthal. БРИЛЛ. ISBN 978-90-04-00617-1.CS1 maint: ref = harv (связь)
- Harwood, Laurence M.; Moody, Christopher J. (1989). Экспериментальная органическая химия: принципы и практика (Иллюстрированный ред.). Оксфорд: Научные публикации Блэквелла. ISBN 978-0-632-02017-1.CS1 maint: ref = harv (связь)
дальнейшее чтение
- Allchin, F. R. (1979). "India: The Ancient Home of Distillation?". мужчина. 14 (1): 55–63. Дои:10.2307/2801640. JSTOR 2801640.
- Needham, Joseph (1980). Наука и цивилизация в Китае. Издательство Кембриджского университета. ISBN 0-521-08573-X.
- Geankoplis, Christie John (2003). Transport Processes and Separation Process Principles (4-е изд.). Прентис Холл. ISBN 978-0-13-101367-4.
внешняя ссылка
- Alcohol distillation
- Case Study: Petroleum Distillation
- "Binary Vapor-Liquid Equilibrium Data" (searchable database). Chemical Engineering Research Information Center. Получено 5 мая 2007.