Синоатриальный узел - Sinoatrial node
| Синоатриальный узел | |
|---|---|
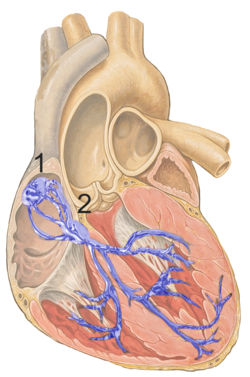 Рисунок 1 показывает проводящая система сердца. Узел SA помечен 1. | |
| Подробности | |
| Система | Система электрической проводимости сердца |
| Артерия | Синоатриальная узловая артерия |
| Идентификаторы | |
| латинский | nodus sinuatrialis |
| Акроним (ы) | Узел SA |
| MeSH | D012849 |
| TA98 | A12.1.06.003 |
| TA2 | 3953 |
| FMA | 9477 |
| Анатомическая терминология | |
В синоатриальный узел (также известный как Узел SA или синусовый узел) - это группа клетки расположен в стене правое предсердие из сердце.[1] Эти клетки обладают способностью самопроизвольно производить электрический импульс (потенциал действия; подробнее см. ниже), который проходит через сердце через система электропроводности (см. рисунок 1), заставляя его договор. В здоровом сердце узел SA постоянно вырабатывает потенциал действия, задавая ритм сердца, и поэтому известен как сердечный естественный кардиостимулятор. На скорость производства потенциала действия (и, следовательно, на частоту сердечных сокращений) влияют: нервы которые его снабжают.[2]
Структура
Синоатриальный узел представляет собой структуру в форме банана, которая различается по размеру, обычно от 10-30 миллиметров (мм) в длину, 5-7 мм в ширину и 1-2 мм в глубину.[3][4]
Место расположения
Узел SA находится в стене (миокард ) из правое предсердие, сбоку от входа в верхняя полая вена в регионе, называемом sinus venarum (следовательно сино- + предсердный ).[5] Он расположен примерно между канавкой, называемой crista terminalis расположен на внутренней поверхности сердце и соответствующие sulcus terminalis, на внешней поверхности.[2] Эти канавки проходят между входом в верхняя полая вена и нижняя полая вена.
Микроанатомия
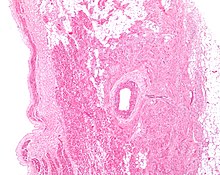
Ячейки узла SA распределены внутри сетки соединительная ткань, содержащий нервы, кровеносный сосуд, коллаген и толстый. Клетки SA-узла непосредственно окружают паранодальные клетки.[2] Эти ячейки имеют структуры, промежуточные между структурами ячеек узла SA и остальной частью Атриум.[6] Соединительная ткань вместе с паранодальными клетками изолируют SA-узел от остальной части предсердия, предотвращая влияние электрической активности предсердных клеток на клетки SA-узла.[2] Ячейки узла SA меньше и светлее окружающих предсердные клетки, при этом средняя ячейка составляет около 8 микрометров в диаметре и 20-30 микрометров в длину (1 микрометр = 0,000001 метр).[7] В отличие от предсердных клеток, клетки SA-узла содержат меньше митохондрии (силовая установка ячейки), меньше миофибры (сократительный аппарат клетки) и меньший саркоплазматический ретикулум (органелла хранения кальция, которая высвобождает кальций для сокращение ). Это означает, что ячейки узла SA менее приспособлены к сокращению по сравнению с предсердный и желудочковый клетки.[8]
Потенциалы действия переходят из одного сердечная клетка к следующей через поры, известные как щелевые соединения. Эти щелевые соединения состоят из белков, называемых коннексины. Внутри узла SA меньше щелевых контактов и они меньше по размеру. Это снова важно для изоляции узла SA от окружающих клеток предсердия.[2][8]
Кровоснабжение
Синоатриальный узел получает кровоснабжение от синоатриальная узловая артерия. Однако это кровоснабжение может сильно различаться у разных людей. Например, у большинства людей это единственный артерия, хотя в некоторых случаях имелось 2 или 3 артерии синоатриального узла, снабжающие СА узел. Кроме того, артерия узла SA в основном берет свое начало как ветвь правая коронарная артерия; однако у некоторых людей он возник из-за огибающая артерия, который является ветвью левая коронарная артерия. Наконец, артерия SA-узла обычно проходит за верхняя полая вена, до достижения узла SA; однако в некоторых случаях он проходит впереди. Несмотря на эти многочисленные различия, похоже, нет никакого преимущества в том, сколько синоатриальных узловых артерий у человека или где они берут начало. [9]
Венозный дренаж
Нет больших вены которые отводят кровь от узла SA. Вместо этого меньше венулы слить кровь прямо в правое предсердие.[10]
Функция
Кардиостимуляция
Основная роль клетки синоатриального узла заключается в инициировании потенциалов действия сердца, которые могут проходить через клетки сердечной мышцы и вызвать сокращение. Потенциал действия - это быстрое изменение мембранный потенциал, вызванные движением заряженных атомов (ионы ). В отсутствие стимуляции клетки без водителя ритма (включая желудочковый и предсердные клетки ) имеют относительно постоянный мембранный потенциал; это известно как потенциал покоя. Эта фаза покоя (см. потенциал сердечного действия, фаза 4 ) заканчивается, когда потенциал действия достигает ячейки. Это приводит к положительному изменению мембранного потенциала, известному как деполяризация, который распространяется по сердцу и инициирует сокращение мышц. Клетки кардиостимулятора, однако, не обладают потенциалом покоя. Вместо этого сразу после реполяризация мембранный потенциал этих клеток снова начинает автоматически деполяризоваться, явление, известное как потенциал кардиостимулятора. Как только потенциал кардиостимулятора достигает заданного значения, пороговый потенциал, он создает потенциал действия.[2] Другие клетки сердца (включая Волокна Пуркинье[11] и атриовентрикулярный узел ) может также инициировать потенциалы действия; однако они делают это с меньшей скоростью, и поэтому, если узел SA функционирует должным образом, его потенциалы действия обычно перекрывают те, которые были бы произведены другими тканями.[12]
Ниже описаны 3 фазы потенциала действия синоатриального узла. в потенциал сердечного действия, существует 5 фаз (обозначенных 0-4), однако потенциалы действия кардиостимулятора не имеют очевидной фазы 1 или 2.
Фаза 4

Эта фаза также известна как потенциал кардиостимулятора. Сразу после реполяризации, когда мембранный потенциал очень отрицательный (он гиперполяризован), напряжение начинает медленно возрастать. Изначально это связано с закрытием калиевые каналы, что уменьшает поток калий ионы (Ik) из ячейки (см. фазу 2 ниже).[13] Гиперполяризация также вызывает активацию активируемые гиперполяризацией циклические нуклеотидно-управляемые каналы (HCN). Активация ионных каналов при очень отрицательных мембранных потенциалах необычна, поэтому поток натрий (Na+) и немного K+ через активированный канал HCN называется смешной ток (Яж).[14] Этот забавный ток заставляет мембранный потенциал клетки постепенно увеличиваться, поскольку положительный заряд (Na+ и K+) течет в ячейку. Другой механизм, связанный с потенциалом кардиостимулятора, известен как кальций Часы. Это относится к спонтанному высвобождению кальция из саркоплазматический ретикулум (запас кальция) в цитоплазму, также известный как искры кальция. Это увеличение кальция в клетке затем активирует натрий-кальциевый обменник (NCX), который удаляет один Ca2+ из ячейки, и обменивает его на 3 Na+ в ячейку (таким образом, снимая с ячейки заряд +2, но позволяя заряду +3 проникнуть в ячейку), дополнительно увеличивая мембранный потенциал. Позже кальций снова попадает в клетку через SERCA и кальциевые каналы расположен на клеточной мембране.[15] Увеличение мембранного потенциала, вызванное этими механизмами, активирует Кальциевые каналы Т-типа а потом Кальциевые каналы L-типа (которые открываются очень медленно). Эти каналы позволяют потоку Ca2+ в клетку, делая мембранный потенциал еще более положительным.
Фаза 0
Это фаза деполяризации. Когда мембранный потенциал достигает порогового значения (от -20 до -50 мВ), клетка начинает быстро деполяризоваться (становиться более положительной).[16] В основном это связано с потоком Ca2+ через кальциевые каналы L-типа, которые теперь полностью открыты. На этом этапе отключаются кальциевые каналы Т-типа и каналы HCN.
Фаза 3
Эта фаза - фаза реполяризации. Это происходит из-за инактивации кальциевых каналов L-типа (предотвращая перемещение Са2+ в клетку) и активация калиевых каналов, что позволяет потоку K+ из клетки, делая мембранный потенциал более отрицательным.[17]
Нервное питание
Частота сердцебиения зависит от скорости, с которой синоатриальный узел производит потенциалы действия. В состоянии покоя частота сердечных сокращений составляет от 60 до 100 ударов в минуту. Это результат активности двух наборов нервов, один из которых замедляет выработку потенциала действия (это парасимпатические нервы ), а другой - для ускорения производства потенциала действия (симпатические нервы ).[18]
Симпатические нервы начинаются в грудной область спинного мозга (в частности Т1-Т4). Эти нервы выделяют нейромедиатор, называемый норадреналин (NA). Это связывается с рецептором на мембране узла SA, называемым бета-1адренорецептор. Связывание NA с этим рецептором активирует G-белок (в частности, граммs-Белок, S для стимуляции), который запускает серию реакций (известных как путь цАМФ ), что приводит к образованию молекулы, называемой циклический аденозинмонофосфат (цАМФ). Этот цАМФ связывается с каналом HCN (см. Выше). Связывание цАМФ с HCN увеличивает поток Na+ и K+ в клетку, ускоряя потенциал кардиостимулятора, тем самым создавая потенциалы действия с большей скоростью и увеличивая частоту сердечных сокращений.[19] Увеличение частоты сердечных сокращений известно как положительное хронотропия.
В парасимпатические нервы поставляющий узел SA (в частности, Блуждающие нервы ) происходят из мозг. Эти нервы выпускают нейромедиатор, называемый ацетилхолин (АХ). ACh связывается с рецептором, называемым М2 мускариновый рецептор, расположенный на мембране СА узла. Активация этого рецептора M2 затем активирует белок, называемый G-белком (в частности, граммя белок, i - тормозной). Активация этого G-белка блокирует путь цАМФ, снижая его эффекты, тем самым подавляя симпатическую активность и замедляя производство потенциала действия. Помимо этого, G-белок также активирует калиевый канал, что позволяет K+ вытекать из клетки, делая мембранный потенциал более отрицательным и замедляя потенциал кардиостимулятора, тем самым снижая скорость производства потенциала действия и, следовательно, снижая частоту сердечных сокращений.[20] Уменьшение частоты сердечных сокращений известно как отрицательное хронотропия.
Первая клетка, которая производит потенциал действия в узле SA, не всегда одна и та же: это называется смещением кардиостимулятора. У некоторых видов животных - например, у собак - высший сдвиг (т. Е. Клетка, которая производит самый быстрый потенциал действия в узле SA выше, чем раньше) обычно вызывает учащение сердечного ритма, тогда как нижний сдвиг (т.е. клетка, производящая потенциал самого быстрого действия в узле SA ниже, чем раньше), вызывает снижение частоты сердечных сокращений.[2]
Клиническое значение
Дисфункция синусового узла описывает нерегулярное сердцебиение, вызванное ошибочными электрическими сигналами сердца. Когда синоатриальный узел сердца дефектен, сердечные ритмы становятся ненормальными - обычно слишком медленными или с паузами в своей функции или комбинации, и очень редко быстрее, чем обычно.[21]
Блокировка артериального кровоснабжения узла SA (чаще всего из-за инфаркт миокарда или прогрессивный ишемическая болезнь сердца ) поэтому может вызвать ишемия и гибель клеток в узле SA. Это может нарушить функцию электрокардиостимулятора в узле SA и привести к синдром слабости синусового узла.
Если узел SA не функционирует или импульс, генерируемый в Узел SA заблокирован Прежде чем он пойдет по системе электропроводности, группа клеток, расположенных дальше по сердцу, станет его кардиостимулятором.[22]
История
Синоатриальный узел был впервые обнаружен молодым студентом-медиком, Мартин Флэк, в самом сердце крот, пока его наставник, сэр Артур Кейт, был на велосипеде со своей женой. Они сделали открытие в импровизированной лаборатории, устроенной на ферме в Кент, Англия, называется Mann's Place. Их открытие было опубликовано в 1907 году.[23][24]
Дополнительные изображения

Сердце; проводящая система (узел SA обозначен 1)
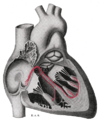
Схематическое изображение атриовентрикулярного пучка
Смотрите также
- Кардиостимулятор
- Кардиология
- Блок сердца
- Синусовая брадикардия
- Синусовая тахикардия
- Кардиоторакальная хирургия
Рекомендации
- ^ Кейт, А; Флэк, М. (1907). «Форма и природа мышечных связей между первичными отделами сердца позвоночных». J Anat Physiol. 41 (3): 172–189. ЧВК 1289112. PMID 17232727.
- ^ а б c d е ж грамм Monfredi, O .; Добжински, H .; Мондаль, Т .; Boyett, M.R .; Моррис, Г. (2010). "Анатомия и физиология синоатриального узла-современный обзор". Электрокардиостимуляция и клиническая электрофизиология. 33 (11): 1392–1406. Дои:10.1111 / j.1540-8159.2010.02838.x. PMID 20946278.
- ^ Csepe, Thomas A .; Чжао, Цзичао; Хансен, Брайан Дж .; Оболочка; Сул, Лидия В .; Лим, Хвала; Ван Юйфэн; Simonetti, Orlando P .; Килич, Ахмет (1 марта 2017 г.). «Структура синоатриального узла человека: трехмерная микроанатомия синоатриальных проводящих путей». Прогресс в биофизике и молекулярной биологии. 120 (1–3): 164–178. Дои:10.1016 / j.pbiomolbio.2015.12.011. ISSN 0079-6107. ЧВК 4808362. PMID 26743207.
- ^ Chandler, N .; Асланиди, О .; Бакли, Д .; Inada, S .; Birchall, S .; Аткинсон, А .; Кирк, Д .; Monfredi, O .; Molenaar, P .; Андерсон, Р .; Sharma, V .; Sigg, D .; Zhang, H .; Boyett, M .; Добжинский, Х. (2011). «Компьютерная трехмерная анатомическая реконструкция синусового узла человека и новой паранодальной области». Анатомическая запись. 294 (6): 970–9. Дои:10.1002 / ar.21379. PMID 21538926.
- ^ Эльзевир, Иллюстрированный медицинский словарь Дорланда, Эльзевир.
- ^ Чендлер, штат Нью-Джерси; Greener, ID; Tellez, JO; Инада, S; Musa, H; Molenaar, P; Дифранческо, Д; и другие. (2009). «Молекулярная архитектура синусового узла человека: понимание функции кардиостимулятора». Тираж. 119 (12): 1562–1575. Дои:10.1161 / cycleaha.108.804369. PMID 19289639.
- ^ Honjo, H .; Boyett, M.R .; Kodama, I .; Тояма, Дж. (1996). «Корреляция между электрической активностью и размером клеток сино-предсердного узла кролика». Журнал физиологии. 496 (3): 795–808. Дои:10.1113 / jphysiol.1996.sp021728. ЧВК 1160865. PMID 8930845.
- ^ а б Boyett, Honjo; Кодама, И. (2000). «Синоатриальный узел, неоднородная структура кардиостимулятора». Сердечно-сосудистые исследования. 47 (4): 658–87. Дои:10.1016 / с0008-6363 (00) 00135-8. PMID 10974216.
- ^ Vikse, J .; Генри, B.M .; Рой, Дж .; Рамакришнан, П.К .; Hsieh, W.C .; Walocha, J.A .; Томашевский, К.А. (2016b). «Анатомические вариации синоатриальной узловой артерии: метаанализ и клинические соображения». PLOS ONE. 11 (2): e0148331. Bibcode:2016PLoSO..1148331V. Дои:10.1371 / journal.pone.0148331. ЧВК 4743947. PMID 26849441.
- ^ Андерсон, К.Р .; Ho, S.Y .; Андерсон, Р.Х. (1979). «Расположение и кровоснабжение синусового узла в сердце человека». Сердце. 41 (1): 28–32. Дои:10.1136 / час.41.1.28. ЧВК 514694. PMID 426954.
- ^ Tsien, R.W .; Карпентер, Д. О. (1 июня 1978 г.). «Ионные механизмы пейсмекерной активности в сердечных волокнах Пуркинье». Слушания Федерации. 37 (8): 2127–2131. ISSN 0014-9446. PMID 350631.
- ^ Вассаль М. (1977). «Взаимосвязь между кардиостимуляторами: подавление перегрузки». Циркуляционные исследования. 41 (3): 269–77. Дои:10.1161 / 01.res.41.3.269. PMID 330018.
- ^ Ирисава, H; Коричневый, ВЧ; Джайлз, В. (1993). «Кардиостимуляция в синоатриальном узле». Physiol Rev. 73 (1): 197–227. Дои:10.1152 / физрев.1993.73.1.197. PMID 8380502.
- ^ ДиФранческо, Д. (2010). «Роль забавного течения в работе кардиостимулятора». Циркуляционные исследования. 106 (3): 434–46. Дои:10.1161 / circresaha.109.208041. PMID 20167941.
- ^ Joung, B .; Chen, P .; Лин, С. (2011). «Роль кальция и часов напряжения в дисфункции синоатриального узла». Йонсей Медицинский журнал. 52 (2): 211–9. Дои:10.3349 / ymj.2011.52.2.211. ЧВК 3051220. PMID 21319337.
- ^ Verkerk, A., Borren, van, Peters, R., Broekhuis, E., Lam, K., Coronel, R., Bakker, de, Tan, H., Wilders, R. (2007) «Отдельные клетки, выделенные из синоатриальный узел человека: потенциалы действия и численная реконструкция тока кардиостимулятора », Материалы конференции: ... Ежегодная международная конференция IEEE Engineering in Medicine and Biology Society. IEEE Engineering in Medicine and Biology Society. Ежегодная конференция., 2007, стр. 904–7.
- ^ Clark, R.B .; Mangoni, M.E .; Lueger, A .; Couette, B .; Nargeot, J .; Джайлз, W.R. (2004). «Быстро активирующийся выпрямитель тока с задержкой K + регулирует активность кардиостимулятора в клетках синоатриального узла взрослых мышей». Американский журнал физиологии. Сердце и физиология кровообращения. 286 (5): 1757–1766. Дои:10.1152 / ajpheart.00753.2003. PMID 14693686.
- ^ Gordan, R .; Gwathmey, J.K .; Се, Л.-Х. (2015). «Вегетативный и эндокринный контроль сердечно-сосудистой функции». Всемирный журнал кардиологии. 7 (4): 204–14. Дои:10.4330 / wjc.v7.i4.204. ЧВК 4404375. PMID 25914789.
- ^ Ларссон, П. (2010) «Как регулируется частота сердечных сокращений в синоатриальном узле? Еще один кусочек головоломки », 136 (3).
- ^ Osterrieder W., Noma A., Trautwein W. (1980) О кинетике калиевого тока, активируемого ацетилхолином в узле SA сердца кролика. Pflügers Arch. 386: 101–109.
- ^ Дисфункция синусового узла Больница горы Синай, Нью-Йорк
- ^ Соединительный ритм в eMedicine
- ^ Silverman, M.E .; Холлман, А. (1 октября 2007 г.). «Открытие синусового узла Китом и Флэком: к столетию их публикации в 1907 году». Сердце. 93 (10): 1184–1187. Дои:10.1136 / час.2006.105049. ЧВК 2000948. PMID 17890694.
- ^ Бойетт М.Р., Добжински Х. (июнь 2007 г.). «Синоатриальный узел все еще задает темп спустя 100 лет после своего открытия». Circ. Res. 100 (11): 1543–5. Дои:10.1161 / CIRCRESAHA.107.101101. PMID 17556667.
внешняя ссылка
- Анатомическая фигура: 20: 06-01 в Human Anatomy Online, Медицинский центр SUNY Downstate - «Проводящая система сердца».
- Схема на gru.net
- урок грудной клетки4 на Уроке анатомии Уэсли Нормана (Джорджтаунский университет) (грудная клетка )
- https://web.archive.org/web/20070929080346/http://www.healthyheart.nhs.uk/heart_works/heart03.shtml


