Дабрафениб - Dabrafenib - Wikipedia
 | |
| Клинические данные | |
|---|---|
| Торговые наименования | Тафинлар |
| Другие имена | ГСК-2118436 |
| AHFS /Drugs.com | Монография |
| MedlinePlus | a613038 |
| Данные лицензии |
|
| Беременность категория |
|
| Маршруты администрация | Устно |
| Код УВД | |
| Легальное положение | |
| Легальное положение | |
| Идентификаторы | |
| |
| Количество CAS | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| КЕГГ | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| Лиганд PDB | |
| Панель управления CompTox (EPA) | |
| ECHA InfoCard | 100.215.965 |
| Химические и физические данные | |
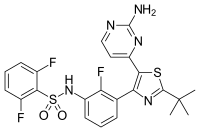
| Формула | C23ЧАС20F3N5О2S2 |
| Молярная масса | 519.56 г · моль−1 |
| 3D модель (JSmol ) | |
| |
| |
Дабрафениб, продается под торговой маркой Тафинлар, это лекарство для лечения рака, связанного с мутированной версией гена BRAF. Дабрафениб действует как ингибитор связанного фермента B-Raf, который играет роль в регуляции рост клеток. Дабрафениб имеет клиническую активность с управляемым профилем безопасности в клинические испытания фазы 1 и 2 у пациентов с метастазами с мутацией BRAF (V600) меланома.[1][2]
Допуски и показания
Соединенные штаты Управление по контролю за продуктами и лекарствами первоначально одобренный дабрафениб как монотерапия для пациентов с BRAF V600E распространенная меланома с положительной мутацией 29 мая 2013 г.[3][4] Дабрафениб был одобрен для использования в Европейском Союзе в августе 2013 года.[5]
Данные клинических испытаний показали, что устойчивость к дабрафенибу и другим ингибиторам BRAF возникает в течение шести-семи месяцев.[6] Чтобы преодолеть эту устойчивость, ингибитор BRAF дабрафениб был объединен с ингибитором MEK. траметиниб.[6] 8 января 2014 г. FDA одобрило эту комбинацию дабрафениба и траметиниба для лечения метастатической меланомы, мутантной по BRAF V600E / K.[7][8] 1 мая 2018 г. FDA одобрило комбинацию дабрафениб / траметиниб в качестве адъювантное лечение для мутированного BRAF V600E, III стадия меланома после хирургическая резекция по результатам COMBI-AD фаза 3 исследования,[9] что делает его первым режимом пероральной химиотерапии, который предотвращает рецидив рака при меланоме с мутацией BRAF и положительными лимфоузлами.[10]
В апреле 2017 года Европейский союз одобрил комбинацию дабрафениба с траметинибом для лечения BRAF V600-положительного прогрессирующего или метастатического немелкоклеточный рак легкого (НМРЛ).[11][12][5]
Рекомендации
- ^ Гибни, Г. Т .; Загер, Дж. С. (2013). «Клиническая разработка дабрафениба при меланоме мутанта BRAF и других злокачественных новообразованиях». Мнение эксперта по метаболизму лекарств и токсикологии. 9 (7): 893–9. Дои:10.1517/17425255.2013.794220. PMID 23621583.
- ^ Huang, T .; Карсы, М .; Чжугэ, Дж .; Чжун, М .; Лю Д. (2013). «B-Raf и ингибиторы: от лавки к постели». Журнал гематологии и онкологии. 6: 30. Дои:10.1186/1756-8722-6-30. ЧВК 3646677. PMID 23617957.
- ^ «Пакет одобрения лекарственного средства: капсулы тафинлар (дабрафениб) NDA №202806». НАС. Управление по контролю за продуктами и лекарствами (FDA). 24 декабря 1999 г.. Получено 10 апреля 2020.
- ^ «Препараты GSK для лечения меланомы пополнили список разрешенных к применению лекарств в США». Рейтер. 30 мая 2013 года.
- ^ а б «Тафинлар ЕПАР». Европейское агентство по лекарствам (EMA). Получено 10 апреля 2020.
- ^ а б Флаэрти, Кейт Т .; Инфанте, Джеффри Р .; Дауд, Адиль; Гонсалес, Рене; Кеффорд, Ричард Ф .; Сосман, Джеффри; Хамид, Омид; Шухтер, Линн; Себон, Джонатан; Ибрагим, Нагеатте; Кудчадкар, Рагини; Burris, Howard A .; Фальчук, Джеральд; Альгази, Ален; Льюис, Карл; Лонг, Джорджина В .; Пузанов, Игорь; Лебовиц, Питер; Сингх, Аджай; Литтл, Шонда; Солнце, Пэн; Оллред, Алисия; Уэлле, Даниэле; Ким, Кевин Б.; Патель, Киран; Вебер, Джеффри (1 ноября 2012 г.). «Комбинированное ингибирование BRAF и MEK при меланоме с мутациями BRAF V600». Медицинский журнал Новой Англии. 367 (18): 1694–703. Дои:10.1056 / NEJMoa1210093. ЧВК 3549295. PMID 23020132.
- ^ «Комбинация дабрафениба и траметиниба одобрена для лечения прогрессирующей меланомы». OncLive. 9 января 2013 г.
- ^ Maverakis E; Корнелиус Л.А.; Боуэн GM; Phan T; Patel FB; Fitzmaurice S; Привет; Burrall B; Duong C; Клоксин AM; Sultani H; Wilken R; Мартинес С.Р .; Патель Ф (2015). «Метастатическая меланома - обзор текущих и будущих вариантов лечения». Acta Derm Venereol. 95 (5): 516–524. Дои:10.2340/00015555-2035. PMID 25520039.
- ^ Лонг, Джорджина В.; Хаушильд, Аксель; Сантинами, Марио; Аткинсон, Виктория; Мандала, Марио; Кьярион-Силени, Ванна; Ларкин, Джеймс; Ньякас, Марта; Дютрио, Кэролайн; Хейдон, Эндрю; Роберт, Кэролайн; Мортье, Лоран; Шахтер, Джейкоб; Шадендорф, Дирк; Lesimple, Тьерри; Пламмер, Рут; Джи, Ран; Чжан, Пинкуань; Мукерджи, Биджойеш; Лего, Джефф; Кеффорд, Ричард; Даммер, Рейнхард; Кирквуд, Джон М. (9 ноября 2017 г.). «Адъювант дабрафениб плюс траметиниб при меланоме с мутацией стадии III». Медицинский журнал Новой Англии. 377 (19): 1813–1823. Дои:10.1056 / NEJMoa1708539. PMID 28891408.
- ^ «FDA одобрило комбинацию адъювантов для лечения BRAF + меланомы». www.medscape.com. WebMD LLC. Получено 2 мая 2018.
- ^ «ЕС одобрил комбинацию дабрафениба / траметиниба для лечения BRAF + NSCLC». Таргетированная онкология. 4 апреля 2017 г.. Получено 10 апреля 2020.
- ^ «Мекинист ЕПАР». Европейское агентство по лекарствам (EMA). Получено 10 апреля 2020.
дальнейшее чтение
- Дин Л. (2017). «Терапия дабрафенибом и генотипы BRAF и G6PD». В Pratt VM, McLeod HL, Rubinstein WS, et al. (ред.). Резюме по медицинской генетике. Национальный центр биотехнологической информации (NCBI). PMID 28809523. Код книжной полки: NBK447415.
внешняя ссылка
- «Дабрафениб». Портал информации о наркотиках. Национальная медицинская библиотека США.
| Этот противоопухолевый или же иммуномодулирующий препарат, средство, медикамент статья - это заглушка. Вы можете помочь Википедии расширяя это. |
